6.已知常温下,KSP(AgCl)=1.8×10-10 mol2•L-2,KSP(AgI)=8.3×10-17mol2•L-2,下列叙述中,正确的是( )
| A. | 常温下,AgCl 在饱和 NaCl 溶液中的 KSP 比在纯水中的 KSP 小 | |
| B. | 向 AgCl 的悬浊液中加入 KI 溶液,沉淀由白色转化为黄色 | |
| C. | 向 AgCl 的饱和溶液中加入 NaCl 晶体,有 AgCl 析出且溶液中 c(Ag+)=c(Cl-) | |
| D. | 将 0.001 mol•L-1 的 AgNO3 溶液滴入 KCl 和 KI 的混合溶液中,一定先产生 AgI 沉淀 |
2.化学与生产、生活、环境密切相关,下列说法中正确的是( )
| A. | 食盐、次氯酸钠溶液均可以将某些病毒氧化而达到消毒的目的 | |
| B. | 大力实施矿物燃料“脱硫、脱硝”技术,可减少酸雨的发生 | |
| C. | 光纤通信使用的光缆的主要成分是晶体Si,太阳能电池使用的材枓主要是SiO2 | |
| D. | 节日燃放的烟花,是碱金属、锶、铂、铁等金属化合物焰色反应所呈现的色彩 |
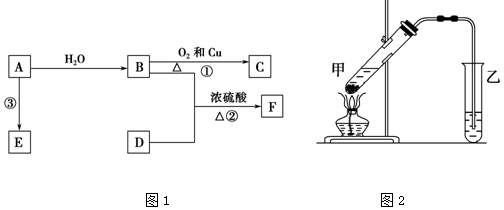
19.X、Y、Z、W为短周期的四种元素,有关它们的部分信息如表所示:
请按要求回答下列问题(注意不能用字母X、Y、Z、W作答):
(1)X单质的电子式是 .
.
(2)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HClO4>HNO3>H2CO3.
(3)W、Z形成的化合物的水溶液的pH<(填“>”“<”或“=”)7,理由是Al3++3H2O?Al(OH)3+3H+ (用离子方程式表示).
(4)8g Y的最简单氢化物完全燃烧生成液态水时放出445kJ的热量,写出Y的最简单氢化物的燃烧热的热化学方程式:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1.
| 元素 | 部分信息 |
| X | X的单质由双原子分子构成,分子中有14个电子 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 |
| Z | Z元素的最高正化合价与最低负化合价的代数和等于6 |
| W | 地壳中含量最多的金属元素 |
(1)X单质的电子式是
 .
.(2)X、Y、Z三种元素的最高价氧化物对应水化物的酸性由强到弱的顺序是:HClO4>HNO3>H2CO3.
(3)W、Z形成的化合物的水溶液的pH<(填“>”“<”或“=”)7,理由是Al3++3H2O?Al(OH)3+3H+ (用离子方程式表示).
(4)8g Y的最简单氢化物完全燃烧生成液态水时放出445kJ的热量,写出Y的最简单氢化物的燃烧热的热化学方程式:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ•mol-1.
18.在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的( )
| A. |  | B. |  | C. |  | D. |  |
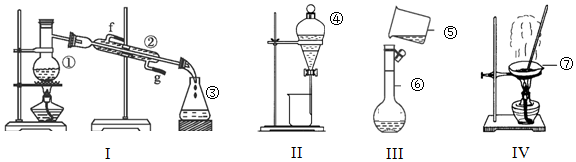
17. 实验室测定常温下l molH2的体积通常用如图所示的装置.
实验室测定常温下l molH2的体积通常用如图所示的装置.
实验记录:温度15℃压强1大气压
(1)求得的平均Vm=23.515L/mol;
(2)实验的相对误差为:0.49%%(已知:15℃时Vm的理论值为:Vm=23.631L/mol).
0 161908 161916 161922 161926 161932 161934 161938 161944 161946 161952 161958 161962 161964 161968 161974 161976 161982 161986 161988 161992 161994 161998 162000 162002 162003 162004 162006 162007 162008 162010 162012 162016 162018 162022 162024 162028 162034 162036 162042 162046 162048 162052 162058 162064 162066 162072 162076 162078 162084 162088 162094 162102 203614
 实验室测定常温下l molH2的体积通常用如图所示的装置.
实验室测定常温下l molH2的体积通常用如图所示的装置.实验记录:温度15℃压强1大气压
| 实验次数 | 镁带质量(g) | 硫酸体积( mL) | 氢气体积( mL) | l摩尔气体的体积(L)(精确到0.001L) |
| 1 | 0.050 | 10 | 49.0 | |
| 2 | 0.049 | 10 | 48.0 |
(2)实验的相对误差为:0.49%%(已知:15℃时Vm的理论值为:Vm=23.631L/mol).