题目内容
5.根据如图所示实验装置,回答下列问题: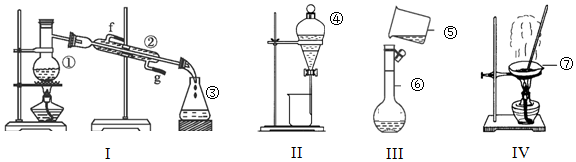
(1)写出下列仪器的名称:②冷凝管,③锥形瓶,⑦蒸发皿.
(2)上述仪器中实验之前需检查装置是否会漏水的是分液漏斗、容量瓶 (填仪器名称)
(3)实验室准备用18mol/L浓硫酸配制100mL 3mol/L稀硫酸.则所需浓硫酸的体积是16.7 mL(保留一位小数),量取浓硫酸所用量筒的规格是25mL(选填“10mL”、“25mL”或“50mL”).在实验操作的摇匀过程中,不慎洒出几滴,此时
应采取的措施是重新配制.若所配制的稀硫酸浓度偏大,则下列可能的原因分析中正确的是BCD.
A.配制前,容量瓶中有少量蒸馏水B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容D.定容时,俯视溶液的凹液面.
分析 (1)依据仪器形状说出仪器名称;
(2)带有活塞或瓶塞的装置使用前要检查是否漏水;
(3)依据溶液稀释过程中溶质的物质的量不变计算需要浓硫酸的体积;依据浓硫酸体积选择量筒规格;
凡是导致实验失败且无法补救的都需要重新配制;
分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
解答 解:(1)依据仪器的形状可知:②冷凝管; ③锥形瓶; ⑦蒸发皿;
故答案为:②冷凝管; ③锥形瓶; ⑦蒸发皿;
(2)容量瓶带有瓶塞、分液漏斗带有活塞使用前应检查是否漏水;
故答案为:分液漏斗、容量瓶;
(3)实验室准备用18mol/L浓硫酸配制100mL 3mol/L稀硫酸,设需要浓硫酸体积为V,则依据溶液稀释过程中溶质的物质的量不变得:18mol/L×V=100mL×3mol/L,解得V=16.7mL;应选择25mL量筒;
在实验操作的摇匀过程中,不慎洒出几滴,导致实验失败,且无法补救必须重新配制;
A.配制前,容量瓶中有少量蒸馏水,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,故A不选;
B.量取浓硫酸时,仰视液体的凹液面,导致量取浓硫酸体积偏大,溶质的物质的量偏大,溶液浓度偏高,故B选;
C.未冷却,立即转移至容量瓶定容,冷却后溶液体积偏小,溶液浓度偏高,故C选;
D.定容时,俯视溶液的凹液面,导致溶液体积偏小,溶液浓度偏高,故D选;
故选:BCD.
点评 本题为实验题,考查了常见仪器名称及使用方法,一定物质的量浓度溶液的配制,熟悉仪器的用途和名称,掌握配制原理是解题关键,题目难度不大.

练习册系列答案
相关题目
1.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 10g质量分数为46%的乙醇水溶液中所含原子数目为0.6NA | |
| B. | 常温常压下,11.2L乙烯所含分子数目小于0.5NA | |
| C. | 常温常压下.4.4gN2O与CO2的混合气体中含的原子数目为0.3NA | |
| D. | 常温下,1molC5H12中含有共价键数为16NA |
16.已知常温下向AgCl饱和溶液中滴加一定浓度的KI溶液,可观察到白色沉淀逐渐变成黄色.由此可知下列有关说法正确的是( )
| A. | 相同温度下,Ksp(AgI)>Ksp(AgCl) | |
| B. | 由于AgCl与AgI的饱和水溶液几乎都不导电说明这两种物质均为非电解质 | |
| C. | 分别用等体积的蒸馏水和0.01 mol/L KI溶液洗涤AgI沉淀,用水洗涤沉淀损失量大 | |
| D. | 将AgCl与AgI的饱和溶液等体积混合后,再加入足量浓AgNO3溶液,只有AgI沉淀生成 |
13.下列措施不利于改善环境质量的是( )
| A. | 在燃煤中添加石灰石以减少酸雨的发生 | |
| B. | 严格执行机动车尾气排放标准 | |
| C. | 将所有垃圾通过露天焚烧、深埋的方式进行处理 | |
| D. | 利用二氧化碳等原料合成聚碳酸酯可降解塑料代替聚乙烯 |
10.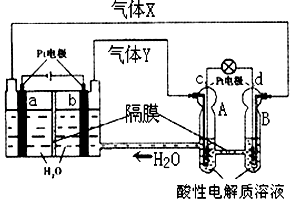 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A. | c极上进行还原反应,B中的H+可以通过隔膜进入A | |
| B. | d极上发生的电极反应是:O2+4H++4e-═2H2O | |
| C. | 该装置开始工作后,右端装置能量变化为:电能→化学能 | |
| D. | 当有0.2mol电子转移时,a极产生1.12L O2 |
17.造成大气污染的SO2主要来源于( )
| A. | 火山喷发 | |
| B. | 自然界中游离态硫缓慢氧化 | |
| C. | 煤、石油等含硫燃料的大量燃烧、硫矿石的冶炼及硫酸工业等产生的工业废气 | |
| D. | 汽车尾气 |
14.下列实验操作能达到实验目的是( )
| 实验操作 | 实验目的 | |
| A | 将SO2通入紫色石蕊溶液中 | 证明SO2具有漂白性 |
| B | 取两支试管,分别加入4mlL0.01mol•L-1KMnO4溶液,然后向另一支试管中加入0.1mol•L-1H2C2O4溶液2mL,向另一支试管中加入0.1mol•L-1H2C2O4溶液4mL,记录褪色时间 | 证明草酸浓度越大,反应速率越快 |
| C | 向10mL0.2mol•L-1NaOH溶液中滴入2滴0.1mol•L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol•L-1FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的溶度积: Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| D | 向含酚酞的Na2SO3溶液中加入BaCl2溶液 | 证明Na2SO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
15.诺氟沙星别名氟哌酸,是治疗肠炎痢疾的常用药.其结构简式如图,下列说法正确的是( )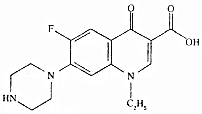

| A. | 该化合物属于苯的同系物 | |
| B. | 分子式为Cl6 H16FN3O3 | |
| C. | 1mol该化合物中含有6NA个双键 | |
| D. | 该化合物能与酸性高锰酸钾、溴水、碳酸氢钠溶液反应 |