19.部分弱酸的电离平衡常数如表:下列选项错误的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 2CN-+H2O+CO2=2HCN+CO32- | |
| B. | 2HCOOH+CO32-=2HCOO-+H2O+CO2↑ | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 | |
| D. | 等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者 |
18.在同温同压下,有同质量的气体甲与乙,已知此时甲的体积小于乙的体积.则下列说法正确的是( )
| A. | 甲的分子数比乙的分子数多 | |
| B. | 甲的摩尔体积比乙的摩尔体积小 | |
| C. | 甲的相对分子质量比乙的相对分子质量大 | |
| D. | 甲的物质的量比乙的物质的量少 |
17.下列有关2L0.2mol•L-1K2SO4溶液的叙述,正确的是( )
| A. | 含有0.2mol K2SO4 | |
| B. | K+的物质的量浓度为0.2mol•L-1 | |
| C. | K的物质的量为0.8mol | |
| D. | 取出1LK2SO4溶液后,剩余K2SO4溶液的浓度变为0.1mol•L-1 |
16.已知CuCl2呈棕色,易溶于水及乙醇和丙酮,其水合物受热分解如下:2CuCl2•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$ Cu(OH)2•CuCl2+2HCl↑+2H2O↑.则下列有关叙述中错误的是( )
| A. | CuCl2具有一定的氧化性 | |
| B. | 电解CuCl2水溶液时,阳极一定得到Cu单质 | |
| C. | Cu(OH)2•CuCl2 属于碱式盐 | |
| D. | 制备无水CuCl2时,需要在HCl气流中加热脱水 |
15.短周期元素X、Y、Z、W的原子序数依次增大,X原子最外层电子数是电子层数的三倍,Y与X可形成Y2X2和Y2X两种离子化合物,Z原子的核外电子数比Y原子多2,W与X同主族,则( )
| A. | 原子半径:Y<Z<W | |
| B. | 单质的还原性:Y<Z | |
| C. | 简单气态氢化物的稳定性:X>W | |
| D. | Y和Z两者最高价氧化物对应的水化物不能相互反应 |
14.下列对化学反应的认识错误的是( )
| A. | 一定会有新物质生成 | B. | 一定伴随着能量的变化 | ||
| C. | 可能会引起物质状态的变化 | D. | 有化学键破坏的一定是化学反应 |
13.有硫酸铁溶液80g,它的密度是dg/cm3,含有2.8gFe3+,则有关该溶液的说法不正确的是( )
| A. | 溶质的质量分数是12.5% | |
| B. | 溶液的物质的量浓度是5d/16mol/L | |
| C. | Fe3+的物质的量浓度是5d/8mol/L | |
| D. | 硫酸根离子的物质的量浓度是10d/16mol/L |
12.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,1L C2H5OH完全燃烧后生成的CO2分子个数约为$\frac{{N}_{A}}{11.2}$ | |
| B. | 通入了1molCl2的新制氯水中,HC1O、Cl一、C1O-粒子数之和为2NA | |
| C. | 含3.0g HCHO的水溶液中原子总数为0.4NA | |
| D. | 3.4gNH3中共用电子对数为0.6NA |
11.向1L含0.3molNaAlO2的溶液中缓慢通入二氧化碳,随n(CO2)增大,下列对应关系不正确的是( )
| 选项 | n(CO2)/mol | 溶液中离子的物质的量浓度 |
| A | 0 | c(Na+)>c(AlO2-)>c(OH-)>c(H+) |
| B | 0.1 | c(Na+)>c(AlO2-)>c(CO32-)>c(OH-)>c(H+) |
| C | 0.2 | c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| D | 0.3 | c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
| A. | A | B. | B | C. | C | D. | D |
10.某化学兴趣小组的同学们对SO2与漂粉精、过氧化钠的反应进行实验探究:
【实验I】SO2与漂粉精反应.
(1)Cl2和Ca(OH)2制取漂粉精的反应中氧化剂与还原剂的物质的量之比为1:1.
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
(3)兴趣小组将A中产生的白雾引出导入硝酸酸化的AgN03溶液中,有沉淀产生,据此判断白雾成分为HCl小液滴,该结论合理吗?不合理请说明理由因为白雾中可能含有少量Cl2和SO2,也容易产生沉淀.
(4)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应.该反应的离子方程式为ClO-+Cl-+2H+=2H2O+Cl2↑.
(5)①将A瓶中混合物过滤、洗涤,得到沉淀X,X的成分是CaSO4(填化学式);
②用离子方程式解释现象3中黄绿色褪去的原因Cl2+SO2+2H2O=4H++2Cl-+SO42-.
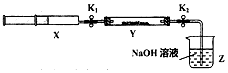
【实验II】SO2与过氧化钠反应.将一定量(过量)SO2充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好.在室温下按图示装置进行实验,请填写空白.
0 161880 161888 161894 161898 161904 161906 161910 161916 161918 161924 161930 161934 161936 161940 161946 161948 161954 161958 161960 161964 161966 161970 161972 161974 161975 161976 161978 161979 161980 161982 161984 161988 161990 161994 161996 162000 162006 162008 162014 162018 162020 162024 162030 162036 162038 162044 162048 162050 162056 162060 162066 162074 203614
【实验I】SO2与漂粉精反应.
| 操作 | 现象 |
| 取4g 漂粉精固体,加入100mL 水 | 部分固体溶解,溶液略有颜色 |
| 过滤,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
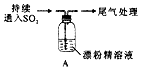 | 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是碱性、漂白性.
(3)兴趣小组将A中产生的白雾引出导入硝酸酸化的AgN03溶液中,有沉淀产生,据此判断白雾成分为HCl小液滴,该结论合理吗?不合理请说明理由因为白雾中可能含有少量Cl2和SO2,也容易产生沉淀.
(4)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl-发生反应.该反应的离子方程式为ClO-+Cl-+2H+=2H2O+Cl2↑.
(5)①将A瓶中混合物过滤、洗涤,得到沉淀X,X的成分是CaSO4(填化学式);
②用离子方程式解释现象3中黄绿色褪去的原因Cl2+SO2+2H2O=4H++2Cl-+SO42-.
【实验II】SO2与过氧化钠反应.将一定量(过量)SO2充入注射器X中,硬质玻璃管Y中加入少量过氧化钠,两端用夹子K1、K2夹好.在室温下按图示装置进行实验,请填写空白.

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中(假设充分反应) | (1)淡黄色固体变为白色粉末 | (2)反应的化学方程式:SO2+Na2O2=Na2SO4 |
| 将注射器活塞退回原处并固定,待装置恢复到室温,打开K2 | (3)Z中NaOH溶液倒吸入Y管中 | (4)不用解释 |