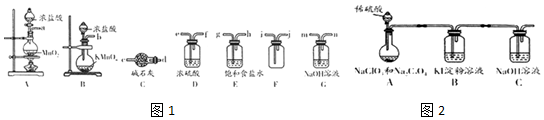
13.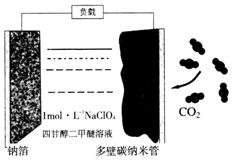 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2═2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2═2Na2CO3+C.下列说法错误的是( )
 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2═2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2═2Na2CO3+C.下列说法错误的是( )| A. | 电池工作温度可能在200℃以上 | |
| B. | 充电时,钠箔与外接电源的负极相连 | |
| C. | 该电池放电时吸收二氧化碳,充电时放出二氧化碳 | |
| D. | 放电时,正极的电极反应为:4Na++3CO2+4e-═2Na2CO3+C |
11.下列关于有机化合物的说法正确的是( )
| A. | C3H6和C4H8互为同系物 | |
| B. | CH2Cl2有2种同分异构体 | |
| C. | 苯乙烯分子中的所有原子不可能处于同一个平面 | |
| D. | 乙酸与乙醇的酯化反应是可逆反应 |
10.下列叙述正确的是( )
| A. | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,溶液呈血红色 | |
| B. | 在溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀,证明原溶液中有Fe2+ | |
| C. | 向FeCl3溶液中滴加稀氨水,可制备Fe(OH)3胶体 | |
| D. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{蒸发、灼烧}{→}$无水FeCl3 |
9.常温下.下列关于电解质溶液的叙述中正确的是( )
| A. | 加水稀释时.在$\frac{c(O{H}^{-})}{C({H}^{+})}$的值增大的溶液中可大量存在:MnO4-、CO32-、K+、NH4+ | |
| B. | 100℃时,将pH=2的硫酸溶液与pH=12的氢氧化钠溶液等体积混合,溶液显中性 | |
| C. | 25℃时,NaB溶液的pH=9,则c(Na+ )-c(B-)=9.9×10-6mol•L-1 | |
| D. | 将0.2mol•L-1 的一元弱酸HA溶液和0.1mol•L-1 的NaOH溶液等体积混合:2c(OH-)+c(A-)=2c(H+)+c(HA) |
8.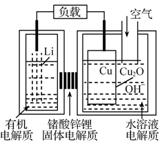 锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
 锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )| A. | 电池放电时,正极附近溶液pH增大 | |
| B. | 工作时,Li+透过固体电解质向Cu极移动 | |
| C. | 电池放电过程中,空气中的O2并不参加反应 | |
| D. | 两极的有机电解质和水溶液电解质不可对换 |
6.25℃时有甲、乙两杯醋酸溶液,甲的pH=2,乙的pH=3,下列判断正确的是( )
| A. | 甲、乙两杯溶液的物质的量浓度之间的关系为c(甲)=10c(乙) | |
| B. | 甲溶液中醋酸的电离程度小 | |
| C. | 中和等物质的量的NaOH,需要乙的体积是甲的10倍 | |
| D. | 甲乙等体积,与足量锌反应时,乙产生氢气的物质的量大 |
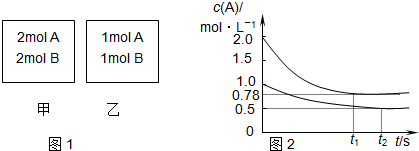
5.向甲、乙两个容积均为1L的恒容容器中,分别充入2mol A、2mol B和1mol A、1mol B.相同条件下(温度为T),发生下列反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是( )
0 161737 161745 161751 161755 161761 161763 161767 161773 161775 161781 161787 161791 161793 161797 161803 161805 161811 161815 161817 161821 161823 161827 161829 161831 161832 161833 161835 161836 161837 161839 161841 161845 161847 161851 161853 161857 161863 161865 161871 161875 161877 161881 161887 161893 161895 161901 161905 161907 161913 161917 161923 161931 203614

| A. | x=1 | |
| B. | 将乙容器单独升温可使乙容器内各物质的体积分数与甲容器内的相同 | |
| C. | 若向甲容器中再充入2 mol A、2 mol B,则平衡时甲容器中:0.78 mol•L-1<c(A)<1.56 mol•L-1 | |
| D. | 若甲容器为等压可变容器,向甲中充入惰性气体,则c(A)减小,平衡正向移动,v(正)、v(逆)减 |