题目内容
13.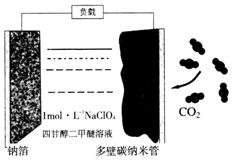 最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2═2Na2CO3+C.下列说法错误的是( )
最近我国科学家发明“可充电钠-二氧化碳电池”(如图),放电时电池总反应为:4Na+3CO2═2Na2CO3+C.下列说法错误的是( )| A. | 电池工作温度可能在200℃以上 | |
| B. | 充电时,钠箔与外接电源的负极相连 | |
| C. | 该电池放电时吸收二氧化碳,充电时放出二氧化碳 | |
| D. | 放电时,正极的电极反应为:4Na++3CO2+4e-═2Na2CO3+C |
分析 二甲醚易挥发,反应在温度较低的环境中进行,原电池工作时,钠为负极,被氧化而失去电子,正极上二氧化碳得电子被还原,发生4Na++3CO2+4e-═2Na2CO3+C,以此解答该题.
解答 解:A.二甲醚易挥发,所以温度不能过高,故A错误;
B.充电时,将钠离子转化为单质钠,发生还原反应是电解池的阴极,所以与外接电源的负极相连,故B正确;
C.放电时,正极上吸收二氧化碳生成碳酸钠,充电时,阳极发生氧化反应,碳被氧化生成二氧化碳,故C正确;
D.放电时正极发生还原反应,二氧化碳中碳得电子生成单质碳,电极反应式为:4Na++3CO2+4e-=2Na2CO3+C,故D正确;
故选A.
点评 本题考查化学电源新型电池,为高频考点,侧重考查学生的分析能力,明确各个电极上发生的反应是解本题关键,知道正负极与阴阳极电极反应式之间的关系,难点是电极反应式的书写.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
3.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法不正确的是( )
| A. | W、Y、R的简单离子半径依次增大 | |
| B. | X、R、Z都可与Y形成两种化合物 | |
| C. | X2Y的热稳定性强于X2R、沸点也高于X2R,但解释的理由不相同 | |
| D. | Z元素分别与X元素和Y元素形成的化合物都是离子晶体,均能与水反应且一定生成了强碱和无色气体 |
4.胃酸的主要成分是( )
| A. | 盐酸 | B. | 醋酸 | C. | 硫酸 | D. | 硝酸 |
1.下列关于油脂的叙述正确的是( )
| A. | 油脂均为固体 | |
| B. | 油脂在体内直接氧化产生热量 | |
| C. | 多吃动物脂肪比多吃植物油有利 | |
| D. | 有些脂肪酸是人体必需的,但在人体内却不能合成;脂肪中必需脂肪酸的含量越高,其营养价值越高 |
8.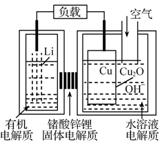 锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
 锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )
锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池工作时发生复杂的铜腐蚀现象,电池总反应为:2Li+Cu2O+H2O═2Cu+2Li++2OH-,其工作原理如图所示,下列说法不正确的是( )| A. | 电池放电时,正极附近溶液pH增大 | |
| B. | 工作时,Li+透过固体电解质向Cu极移动 | |
| C. | 电池放电过程中,空气中的O2并不参加反应 | |
| D. | 两极的有机电解质和水溶液电解质不可对换 |
6.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,4-丁二烯 | B. |  3-丁醇 3-丁醇 | ||
| C. |  甲基苯酚 甲基苯酚 | D. |  2-甲基丁烷 2-甲基丁烷 |
3.化学与生产、生活、科技等密切相关,下列说法不正确的是( )
| A. | 加大清洁能源的开发利用,提髙资源的利用率 | |
| B. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| C. | 用K2FeO4取代Cl2处理饮用水,可杀菌消毒,还能沉降水中的悬浮物 | |
| D. | 用沼气、太阳能、风能等新型能源代替化石燃料 |
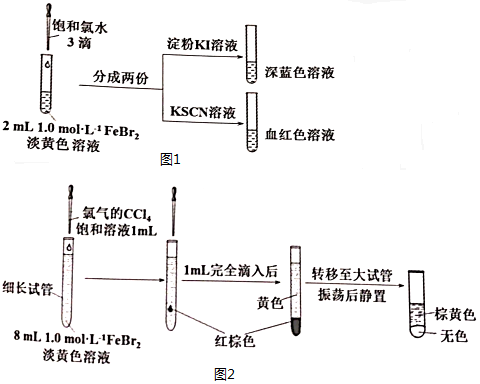
4.下列实验现象描述正确的是( )
| A. | 红热的铜丝在硫蒸汽中燃烧,产生黑色固体 | |
| B. | 碘水中加入少量CCl4,振荡静置后,下层颜色变浅,上层颜色变为紫色 | |
| C. | 往溴水中加入碘化钠溶液,溴水变为无色 | |
| D. | 氢气在Cl2中燃烧产生白色的烟 |