14.现有一硝酸钾固体样品,其中含有的杂质为可溶性的Ca(NO3)2、Mg(NO3)2、K2SO4等,通过如下几个实验步骤,可制得不含杂质的硝酸钾溶液:①加入稍过量的K2CO3溶液:②加入稍过量的KOH溶液;③加入稍过量的Ba(NO3)2溶液;④滴入稀硝酸至无气泡产生;⑤过滤,其中正确的操作顺序是( )
| A. | ③②①⑤④ | B. | ①②③④⑤ | C. | ②③①④⑤ | D. | ③⑤②①④ |
12.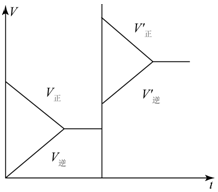 对于达平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速度(v)的变化如图,分析可知X、Y、Z,W的聚集状态可能是( )
对于达平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速度(v)的变化如图,分析可知X、Y、Z,W的聚集状态可能是( )
 对于达平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速度(v)的变化如图,分析可知X、Y、Z,W的聚集状态可能是( )
对于达平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速度(v)的变化如图,分析可知X、Y、Z,W的聚集状态可能是( )| A. | Z、W为气体,X、Y中之一为气体 | B. | X、Y中之一为气体,Z、W为非气体 | ||
| C. | X、Y、Z、W皆为气体 | D. | X、Y为气体,Z、W中之一为气体 |
11.在一定温度下,向aL密闭的容器中加入1 molX气体和1 molY气体,发生如下反应:X(g)+Y(g)?2Z(g)此反应达到平衡的标志是( )
| A. | 容器内压强不随时间变化 | |
| B. | 容器内各物质的浓度不随时间变化 | |
| C. | 容器内各物质X、Y、Z的浓度之比为1:1:2 | |
| D. | 单位时间内消耗0.1 molX,同时生成0.2 molZ |
10.下列反应中硫酸既表现氧化性,又表现出酸性的是( )
| A. | 实验室用浓硫酸干燥氯气、氯化氢等气体 | |
| B. | 将KI与浓硫酸混合,有紫色蒸气产生 | |
| C. | 浓硫酸与氧化铁反应,生成硫酸铁 | |
| D. | 用浓硫酸在木制品上“烙”字画 |
8.下列离子方程式中正确的是( )
| A. | 少量SO2通入过量氨水中:NH3•H2O+SO2→HSO3-+NH4+ | |
| B. | H2S通入氯水中:S2-+Cl2→S↓+2Cl- | |
| C. | 二氧化氮溶于水:3NO2+H2O→2H++2NO3-+NO | |
| D. | 少量NaHSO4与过量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-→BaSO4↓+2H2O |
7.下列各组数据关系中,前者比后者大的是( )
| A. | 纯水100℃和25℃的pH值 | |
| B. | 氢硫酸溶液中的H+和HS-的浓度 | |
| C. | 100mL0.1mol/L的CH3COOH溶液与10mL1.0mol/L的CH3COOH溶液中H+数目 | |
| D. | 25℃,pH=11的KOH溶液与pH=3的CH3COOH溶液中由水电离出的OH-离子浓度 |
6.反应A(g)+2B(g)?C(g)+D(g)+QKJ的能量变化如图所示,有关叙述正确的是( )
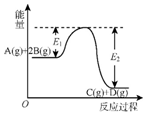

| A. | Q=E2 | |
| B. | 在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 | |
| C. | Q>0,升高温度,正反应速率增大,逆反应速率减小 | |
| D. | 若减小体积,平衡会移动,当反应再次达到平衡时,A的平衡浓度增大 |
5.使用单质铜制取硝酸铜,最适宜的方法是( )
0 161502 161510 161516 161520 161526 161528 161532 161538 161540 161546 161552 161556 161558 161562 161568 161570 161576 161580 161582 161586 161588 161592 161594 161596 161597 161598 161600 161601 161602 161604 161606 161610 161612 161616 161618 161622 161628 161630 161636 161640 161642 161646 161652 161658 161660 161666 161670 161672 161678 161682 161688 161696 203614
| A. | Cu+稀HNO3 | B. | Cu$\stackrel{空气、△}{→}$CuO$\stackrel{硝酸}{→}$Cu(NO3)2 | ||
| C. | Cu+浓HNO3 | D. | Cu$\stackrel{Cl_{2}}{→}$CuCl2 $\stackrel{AgNO_{3}}{→}$ Cu(NO3)2 |
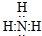 ,氯化铵
,氯化铵 .
.