16.下列实验“操作和现象”与“结论”及对应关系均正确的是( )
| 实验操作、现象 | 实验结论 | |
| A | 将FeCl3溶液分别滴入NaBr、NaI溶液中,再分别滴加CCl4,振荡,静置后CCl4层均有颜色 | 氧化性:Fe3+>Br2>I2 |
| B | 向某溶液中加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量SO42- |
| C | 将SO2通入溴水中,溴水褪色 | SO2具有漂白性 |
| D | 除锈的铁钉在浓硝酸中浸泡后,用蒸馏水洗净,再放入CuSO4溶液中无现象 | 铁钉表面形成了一层致密稳定的氧化膜 |
| A. | A | B. | B | C. | C | D. | D |
15.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )
| A. | 负极的反应式为:Zn2+-2e-=Zn | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
14.常温下,下列离子在指定溶液中一定能大量共存的是( )
| A. | 某无色透明溶液中:Fe2+、Al3+、NO3-、Cl-、S2- | |
| B. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、Cl- | |
| C. | 0.1 mol•L-1的NaHCO3溶液中:K+、Na+、SO42-、CO32- | |
| D. | 加入Mg能放出H2的溶液中:Mg2+、NH4+、ClO-、K+、SO42- |
13.在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入a mol及b mol碘化氢(a>b),待反应2HI(g)?I2(g)+H2(g) 达平衡后,下列说法正确的是( )
| A. | 平衡时两容器中I2的物质的量相等 | |
| B. | 平衡时两容器中I2的浓度相等 | |
| C. | 平衡时碘蒸气在混合气体中的百分含量:A容器大于B容器 | |
| D. | 平衡时HI的分解率:αA=αB |
12.下列说法正确的是( )
| A. | 铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓海轮腐蚀 | |
| B. | 钢铁在潮湿空气中生锈,主要发生的是吸氧腐蚀,铁锈的成分是Fe2O3•XH2O | |
| C. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| D. | 吸热反应TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)在一定条件下可自发进行,则该反应的△S<0 |
11.对下列化学用语的理解和描述均正确的是( )
| A. | 电子式 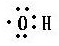 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| B. | 比例模型  可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 | |
| C. | 结构示意图为  的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 | |
| D. | 原子结构示意图 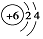 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
9.已知化学方程式:a CuSO4+b FeS2+c H2O=d Cu2S+e FeSO4+f H2SO4,则每当1molCuSO4参加反应,转移的电子数为( )
| A. | 1.5mol | B. | 2mol | C. | 2.5mol | D. | 3mol |
8.标准状况下,700L氨气溶于1L水得到密度为0.9g/cm3的饱和氨水,则该氨水的物质的量浓度约为( )
| A. | 16.4mol/L | B. | 17.4mol/L | C. | 18.4mol/L | D. | 19.4mol/L |
7.下列各物质在反应中做为反应物时仅能体现还原性的是( )
0 160761 160769 160775 160779 160785 160787 160791 160797 160799 160805 160811 160815 160817 160821 160827 160829 160835 160839 160841 160845 160847 160851 160853 160855 160856 160857 160859 160860 160861 160863 160865 160869 160871 160875 160877 160881 160887 160889 160895 160899 160901 160905 160911 160917 160919 160925 160929 160931 160937 160941 160947 160955 203614
| A. | 金属钠 | B. | 稀盐酸 | C. | 硫酸铜 | D. | 氯酸钾 |