题目内容
15.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )| A. | 负极的反应式为:Zn2+-2e-=Zn | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
分析 某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液,原电池发生工作时,Zn被氧化,为原电池的负极,K2FeO4具有氧化性,为正极,碱性条件下被还原生成Fe(OH)3,结合电极方程式以及离子的定向移动解答该题.
解答 解:A.负极发生氧化反应,电极反应式为:Zn-2e-=Zn2+,故A错误;
B.KOH溶液为电解质溶液,则正极电极方程式为2FeO42-+6e-+8H2O=2Fe(OH)3+10OH-,故B错误;
C.该电池放电过程中电解质溶液浓度减小,故错误;
D.电池工作时阴离子OH-向负极迁移,故D正确.
故选D.
点评 本题考查原电池知识,为2016年海南高考题,侧重考查学生的分析能力,题目较为基础,注意从元素化合价的角度分析,把握原电池与氧化还原反应的关系,难度不大.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
5.下列实验操作正确的是( )
| A. | 用滴管滴加液体时,为防止液体滴到试管外面,滴管应紧贴管内壁 | |
| B. | 量筒里装一定量水,沿时筒内壁缓缓倒入浓硫酸,边倒边搅拌,配制稀硫酸 | |
| C. | 皮肤上不慎沾洒上了浓硫酸,应先用水冲洗,再涂上一层氢氧化钠溶液 | |
| D. | 称量易潮解的药品时药品应放在小烧杯等容器中称量 |
6.下列说法正确的是( )
| A. | 碳酸钙难溶于水,放入水中,液体也不导电,所以碳酸钙是非电解质 | |
| B. | 硫酸钡在水中溶解度很小,所以它是弱电解质 | |
| C. | 向1mol•L-1的MgCl2溶液中加入等体积的2mol•L-1 NaOH 溶液后,液体中c(Mg2+)为0 | |
| D. | 向氯化钙的浓溶液中加入浓烧碱溶液,溶液会变浑浊 |
3.下列各项与胶体性质无关的是( )
| A. | 卤水点豆腐 | B. | 明矾净水 | ||
| C. | 静电除尘 | D. | 盐酸与氢氧化钠溶液发生中和反应 |
4.在无色透明强酸性溶液中,能大量共存的离子组是( )
| A. | K+、Cu2+、NO3-、SO42- | B. | K+、Na+、Cl-、ClO- | ||
| C. | Zn2+、NH4+、NO3-、Cl- | D. | K+、Na+、Ca2+、SO42- |
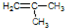 .
. .该分子的所有碳原子能否在一个平面上(填“能”或“不能”)不能.
.该分子的所有碳原子能否在一个平面上(填“能”或“不能”)不能. +3Br2→
+3Br2→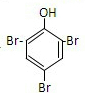 +3HBr
+3HBr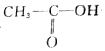 +H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O
+H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O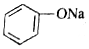 +CO2+H2O→C6H5OH+NaHCO3.
+CO2+H2O→C6H5OH+NaHCO3.