题目内容
10.写出下列反应的离子方程式:(1)实验室用石灰石和稀盐酸制 CO2CaCO3 +2H+=Ca2++H2O+CO2↑.
(2)向 Ba(OH)2溶液中,逐滴加入 NaHSO4溶液使钡离子刚好完全沉淀Ba2++OH-+H++SO42-=BaSO4↓+H2O.
分析 (1)碳酸钙与盐酸反应生成氯化钙和水、二氧化碳;
(2)向 Ba(OH)2溶液中,逐滴加入 NaHSO4溶液使钡离子刚好完全沉淀,氢氧化钡与硫酸氢钠物质的量之比为1:1,反应生成硫酸钡、氢氧化钠和水;
解答 解:(1)碳酸钙与盐酸反应生成氯化钙和水、二氧化碳,离子方程式:CaCO3 +2H+=Ca2++H2O+CO2↑;
故答案为:CaCO3 +2H+=Ca2++H2O+CO2↑;
(2)向 Ba(OH)2溶液中,逐滴加入 NaHSO4溶液使钡离子刚好完全沉淀,氢氧化钡与硫酸氢钠物质的量之比为1:1,反应生成硫酸钡、氢氧化钠和水,离子方程式:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
点评 本题考查了离子方程式的书写,明确物质的性质及发生反应是解题关键,题目难度不大,注意化学式拆分.

练习册系列答案
相关题目
20.下列有关实验原理或实验操作正确的是( )

| A. | 可以用pH试纸测饱和氯水的pH | |
| B. | 用量筒量取8.61 mL 0.1 mol•L-1盐酸 | |
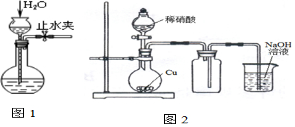
| C. | 用图1所示的操作检查装置的气密性 | |
| D. | 实验室用图2所示的装置制取少量的NO |
18.下列各项说法正确的是( )
| A. | 白磷应放在冷水中保存 | B. | 将水注入浓硫酸中以稀释浓硫酸 | ||
| C. | 硝酸银放在无色试剂瓶中保存 | D. | 在蒸发皿中加热分解氯酸钾固体 |
5.用 NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,含有 NA个氮原子的氮气体积约为 11.2L | |
| B. | 标准状况下,64gSO2中含有的原子数为 3NA | |
| C. | 在常温常压下,11.2L Cl2含有的分子数为 0.5NA | |
| D. | 标准状况下,11.2L H2O 含有的分子数为 0.5NA |
15.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液.下列说法正确的是( )
| A. | 负极的反应式为:Zn2+-2e-=Zn | |
| B. | 正极反应式为2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C. | 该电池放电过程中电解质溶液浓度不变 | |
| D. | 电池工作时OH-向负极迁移 |
19. 密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
i.CO(g)+2H2(g)?CH3OH(g)△H1=-90.1kJ•mol-1
ii.2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24.5kJ•mol-1
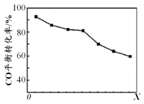
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如图所示.下列说法正确的是( )
 密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:
密闭容器中,由H2和CO直接制备二甲醚(CH3OCH3),其过程包含以下反应:i.CO(g)+2H2(g)?CH3OH(g)△H1=-90.1kJ•mol-1
ii.2CH3OH(g)?CH3OCH3(g)+H2O(g)△H2=-24.5kJ•mol-1
当其他条件相同时,由H2和CO直接制备二甲醚的反应中,CO平衡转化率随条件X 的变化曲线如图所示.下列说法正确的是( )
| A. | 由H2和CO直接制备二甲醚的反应为放热反应 | |
| B. | 条件X为压强 | |
| C. | X增大,二甲醚的产率一定增大 | |
| D. | X增大,该反应的平衡常数一定减小 |
20.下列实验装置图正确且能达到实验目的是( )
| A. | 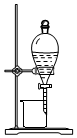 如图所示装置可从碘的CCl4溶液中分离出碘 | |
| B. | 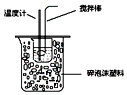 如图所示装置可用于在实验室测定中和反应的反应热 | |
| C. | 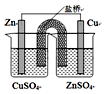 如图所示装置能构成锌铜原电池 | |
| D. | 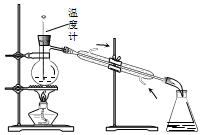 如图所示装置可用于实验室中分馏石油 |