16.自来水常用氯气进行消毒,某实验室用自来水配制下列物质的溶液,会产生明显药品变质问题的是:①FeCl2②AgNO3 ③Na2CO3 ④NaOH⑤石蕊试液( )
| A. | ①②④ | B. | ②③⑤ | C. | ②④⑤ | D. | 全部 |
14.松花蛋于明朝初年问世.其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl).将一定比例的配料用水和粘土调制成糊状,敷于蛋上,密封保存,数日后可食用.
(1)腌制皮蛋配料用水调制时,主要发生化学反应的方程式有CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)皮蛋外的糊状物经溶解、过渡后,所得滤液中肯定大量含有的物质为NaCl和NaOH,可能含有的物质为Ca(OH)2或Na2CO3.
(3)某学生设计如表示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮助他完成实验方案.
(1)腌制皮蛋配料用水调制时,主要发生化学反应的方程式有CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)皮蛋外的糊状物经溶解、过渡后,所得滤液中肯定大量含有的物质为NaCl和NaOH,可能含有的物质为Ca(OH)2或Na2CO3.
(3)某学生设计如表示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮助他完成实验方案.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量滤液,滴加过量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 |
| 若无白色沉淀 | 滤液中无Ca(OH)2 | |
| ②取少量滤液, 滴入过量盐酸 | 若出现 气泡 | 滤液中含Na2CO3 |
| 若无现象 | 滤液中无Na2CO3 |
11.在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,此混合气体中C和O两种原子的物质的量之比为( )
| A. | 3:4 | B. | 4:3 | C. | 2:1 | D. | 1:2 |
10.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入NaOH溶液,产生白色沉淀,一定有Mg2+ | |
| D. | 在试样中先加入HCL无明显现象,再滴加BaCL2,若生成白色沉淀,试样中有SO42- |
9.分类是化学研究中常用的方法,下列分类说法中正确的是( )
| A. | 电离产生阳离子全部是H+化合物叫酸,根据其分子中氢原子的个数确定该酸的元数 | |
| B. | 依据组成元素的种类,将纯净物分为单质和化合物 | |
| C. | 根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物和酸性氧化物 | |
| D. | 根据分散质微粒直径大小,将分散系分为胶体、浊液和溶液 |
8.下列反应不属于氧化还原反应的是( )
| A. | 2HClO=2HCl+O2↑ | B. | Zn+CuSO4=Cu+ZnSO4 | ||
| C. | 2NaOH+H2SO4=Na2SO4+2H2O | D. | H2+F2=2HF |
7.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
0 160755 160763 160769 160773 160779 160781 160785 160791 160793 160799 160805 160809 160811 160815 160821 160823 160829 160833 160835 160839 160841 160845 160847 160849 160850 160851 160853 160854 160855 160857 160859 160863 160865 160869 160871 160875 160881 160883 160889 160893 160895 160899 160905 160911 160913 160919 160923 160925 160931 160935 160941 160949 203614
| A. | 1molNH4Cl所含原子数为2NA | |
| B. | 20克氖气所含原子数约为6.02×1023 | |
| C. | 标准状况下22.4L水所含的分子数为NA | |
| D. | 在20℃、1.01×105Pa时,11.2L氮气含有2NA个氮原子 |
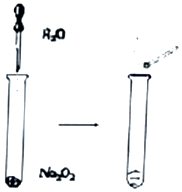 Na2O2具有强氧化性,可以用来漂白纺织累物品、麦秆、纤维等.
Na2O2具有强氧化性,可以用来漂白纺织累物品、麦秆、纤维等.