题目内容
11.在标准状况下,由CO和CO2组成的混合气体13.44L,质量为20g,此混合气体中C和O两种原子的物质的量之比为( )| A. | 3:4 | B. | 4:3 | C. | 2:1 | D. | 1:2 |
分析 根据n=$\frac{V}{{V}_{m}}$计算混合气体的物质的量,令CO和CO2的物质的量分别为xmol、ymol.根据二者物质的量计算出混合气体中C和O两种原子的物质的量之比,由此分析解答.
解答 解:在标准状况下,13.44LCO和CO2组成的混合气体的物质的量为$\frac{13.44L}{22.4L/mol}$=0.6mol,
令CO和CO2的物质的量分别为xmol、ymol,则:x+y=0.6,28x+44y=20,
解得:x=0.4,y=0.2.
所以混合气体中C和O两种原子的物质的量之比为(0.4+0.2):(0.4+2×0.2)=3:4;
故选:A.
点评 本题考查化学计算,难度不大,可以利用十字交叉法计CO与CO2的物质的量之比,再进行计算.

练习册系列答案
相关题目
2.下列物质属于纯净物的是( )
| A. | 石油 | B. | 空气 | C. | 盐酸 | D. | 液氯 |
19.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 将78gNa2O2与过量CO2反应转移的电子数为2NA | |
| B. | 1mol N2与 4mol H2反应生成的NH3 分子数为2NA | |
| C. | 标准状况下,2.24L SO3中所含原子数为0.4 NA | |
| D. | 标准状况下,18g D2O中所含电子数为9 NA |
6.下列溶液中c(Cl-)与50mL1mol•L-1AlCl3溶液中c(Cl-)相等的是( )
| A. | 150mL2mol•L-1的KCl溶液 | B. | 75mL4mol•L-1的NH4Cl溶液 | ||
| C. | 75mL1.5mol•L-1MgCl2溶液 | D. | 150mL1mol•L-1的NaCl溶液 |
16.自来水常用氯气进行消毒,某实验室用自来水配制下列物质的溶液,会产生明显药品变质问题的是:①FeCl2②AgNO3 ③Na2CO3 ④NaOH⑤石蕊试液( )
| A. | ①②④ | B. | ②③⑤ | C. | ②④⑤ | D. | 全部 |
3.NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 18gH2O中含的质子数为10NA | |
| B. | 1.7克H2O2中含有的电子数为0.9 NA | |
| C. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1 mol Na 与足量O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子 |
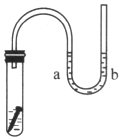 如图所示,试管中放一枚铁钉,并盛放一定量的NaCl溶液,导管中有少量蒸馏水.
如图所示,试管中放一枚铁钉,并盛放一定量的NaCl溶液,导管中有少量蒸馏水.