题目内容
9.分类是化学研究中常用的方法,下列分类说法中正确的是( )| A. | 电离产生阳离子全部是H+化合物叫酸,根据其分子中氢原子的个数确定该酸的元数 | |
| B. | 依据组成元素的种类,将纯净物分为单质和化合物 | |
| C. | 根据氧化物中是否含有金属元素,将氧化物分为碱性氧化物和酸性氧化物 | |
| D. | 根据分散质微粒直径大小,将分散系分为胶体、浊液和溶液 |
分析 A.酸:电离时生成的阳离子全部是H+的化合物;根据酸能电离出H+的个数分类为一元酸、二元酸等;
B.同种元素组成的纯净物为单质,不同种元素组成的纯净物为化合物;
C.根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物;
D.分散系分为溶液、胶体和浊液的本质区别是分散系分散质微粒大小.
解答 解:A.电离时生成的阳离子全部是H+的化合物是酸,根据酸能电离出H+的个数分类为一元酸、二元酸等,而不是关键分子中氢原子的个数,故A错误;
B.同种元素组成的纯净物为单质,不同种元素组成的纯净物为化合物,根据组成元素的种类将纯净物分为单质和化合物,故B错误;
C.根据氧化物的性质将氧化物分成酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物,含金属元素的氧化物可能为碱性氧化物如CaO、两性氧化物如Al2O3、酸性氧化物如Mn2O7,故C错误;
D.根据分散系分散质微粒大小将分散系分为溶液、胶体和浊液,故D正确;
故选D.
点评 本题考查物质的分类,题目难度不大,注意物质的分类的依据,不同的分类标准会得出不同的分类结果.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
17.为达到表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.
供选择的化学试剂及实验方法A.将气体通入盛有NaOH溶液的洗气瓶B.取样,滴加KSCN溶液C.取样,滴加酚酞试液D.取样,灼烧.
供选择的化学试剂及实验方法A.将气体通入盛有NaOH溶液的洗气瓶B.取样,滴加KSCN溶液C.取样,滴加酚酞试液D.取样,灼烧.
| 实验 目 的 | 试剂及方法 |
| 鉴别丝绸和棉布 | |
| 除去CO中混有少量CO2 | |
| 证明Na2CO3溶液呈碱性 | |
| 检验溶液中是否含Fe3+ |
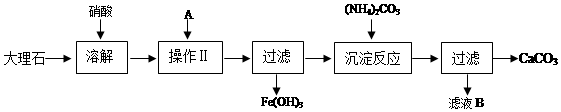
14.松花蛋于明朝初年问世.其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl).将一定比例的配料用水和粘土调制成糊状,敷于蛋上,密封保存,数日后可食用.
(1)腌制皮蛋配料用水调制时,主要发生化学反应的方程式有CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)皮蛋外的糊状物经溶解、过渡后,所得滤液中肯定大量含有的物质为NaCl和NaOH,可能含有的物质为Ca(OH)2或Na2CO3.
(3)某学生设计如表示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮助他完成实验方案.
(1)腌制皮蛋配料用水调制时,主要发生化学反应的方程式有CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
(2)皮蛋外的糊状物经溶解、过渡后,所得滤液中肯定大量含有的物质为NaCl和NaOH,可能含有的物质为Ca(OH)2或Na2CO3.
(3)某学生设计如表示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮助他完成实验方案.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量滤液,滴加过量K2CO3溶液 | 若出现白色沉淀 | 滤液中含Ca(OH)2 |
| 若无白色沉淀 | 滤液中无Ca(OH)2 | |
| ②取少量滤液, 滴入过量盐酸 | 若出现 气泡 | 滤液中含Na2CO3 |
| 若无现象 | 滤液中无Na2CO3 |
1.下列关于溶液和胶体的叙述,正确的是( )
| A. | 溶液是呈电中性的,胶体是带电的 | |
| B. | 通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 | |
| C. | 胶体的分散质可以通过过滤从分散剂中分离出来 | |
| D. | 胶体与其他分散系最本质的区别是:胶体粒子直径介于(1---100 )nm之间 |
18.常温下,在溶液中能发生如下反应:①2A2++B2=2A3++2B-;②16H++10Z-+2XO4-?2X2++5Z2+8H2O③2B-+Z2=B2+2Z-,由此判断下列说法错误的是( )
| A. | Z2+2A2+=2A3++2Z-反应可以进行 | |
| B. | Z元素在②③反应中均被还原 | |
| C. | 氧化性由强到弱的顺序是XO4-、Z2、B2、A3+ | |
| D. | 还原性由强到弱顺序是A2+、B-、Z-、X2+ |
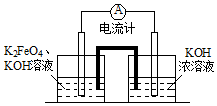 2014年我国的冶金行业深受经济危机的冲击,尤其是Al、Fe的价格下滑幅度很大.请完成下面问题:
2014年我国的冶金行业深受经济危机的冲击,尤其是Al、Fe的价格下滑幅度很大.请完成下面问题: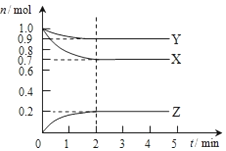 某温度时,在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时,在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析: