题目内容
12.有以下几种物质:①Cu(OH)2②乙醇 ③铜 ④二氧化碳⑤冰醋酸(纯醋酸晶体)⑥KNO3溶液⑦NaHCO3填空回答(填序号):(1)以上物质可以导电的是③⑥;
(2)以上物质中属于电解质的是①⑤⑦;
(3)以上物质中属于非电解质的是②④;
(4)既不是电解质,也不是非电解质③⑥.
分析 水溶液中或熔融状态下能够导电的化合物称为电解质,酸、碱、盐都是电解质;在上述两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物不管在水溶液中或熔融状态下能够导电与否,都不是电解质或非电解质.能导电的物质--必须具有能自由移动的带电的微粒,金属能导电--是由于金属中存在能自由移动的带负电的电子,单质、混合物等既不是电解质,也不是非电解质.
解答 解:(1)能导电的物质--必须具有能自由移动的带电的微粒,Cu中存在能自由移动的带负电的电子能导电,KNO3溶液中有能自由移动的正负离子,也能导电,
故答案为:③⑥;
(2)电解质是在水溶液中或熔融状态下能够导电的化合物,:①Cu(OH)2,⑤冰醋酸(纯醋酸晶体),⑦NaHCO3符合,故答案为:①⑤⑦;
(3)非电解质是在水溶液中或熔融状态下都不能能够导电的化合物,②乙醇,④二氧化碳不能电离属于非电解质,故答案为:②④;
(4)既不是电解质,也不是非电解质的为:③铜,⑥KNO3溶液,故答案为:③⑥.
点评 本题要注意电解质和非电解质都是针对化合物而言的,单质、混合物既不是电解质也不是非电解质,题目难度不大.

练习册系列答案
相关题目
2.下列有关化学用语的表示正确的是( )
| A. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | B. | Al3+的结构示意图: | ||
| C. | NaClO的电子式: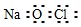 | D. | 对羟基苯甲醛的结构简式: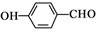 |
3.下列物质包装时应贴上图标志的是( )


| A. | 食盐 | B. | 汽油 | C. | 小苏打 | D. | 烧碱 |
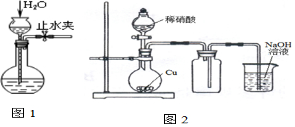
20.下列有关实验原理或实验操作正确的是( )

| A. | 可以用pH试纸测饱和氯水的pH | |
| B. | 用量筒量取8.61 mL 0.1 mol•L-1盐酸 | |
| C. | 用图1所示的操作检查装置的气密性 | |
| D. | 实验室用图2所示的装置制取少量的NO |
7.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1molNH4Cl所含原子数为2NA | |
| B. | 20克氖气所含原子数约为6.02×1023 | |
| C. | 标准状况下22.4L水所含的分子数为NA | |
| D. | 在20℃、1.01×105Pa时,11.2L氮气含有2NA个氮原子 |
17.下列各种酸性氧化物与其对应酸的化学式书写正确的是( )
| A. | SO2→H2SO4 | B. | SO3→H2SO4 | C. | NO2→HNO3 | D. | CO→H2CO3 |
4.下列实验过程的评价,正确的是( )
| A. | 某固体加入稀盐酸,产生了无色气体,证明该固体中一定含有CO32- | |
| B. | 某溶液中滴加BaCl2溶液后,生成不溶于稀HNO3的白色沉淀,该溶液中一定含有SO42- | |
| C. | 某溶液中滴加Ba(OH)2溶液后,生成白色沉淀,该溶液中一定含有SO42- | |
| D. | 要证明烧碱溶液中是否含有氯离子,先加硝酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含有氯离子 |