题目内容
7.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 1molNH4Cl所含原子数为2NA | |
| B. | 20克氖气所含原子数约为6.02×1023 | |
| C. | 标准状况下22.4L水所含的分子数为NA | |
| D. | 在20℃、1.01×105Pa时,11.2L氮气含有2NA个氮原子 |
分析 A.1molNH4Cl含原6mol原子;
B.根据稀有气体为单原子分子进行判断;
C.气体摩尔体积使用对象为气体;
D.20℃、1.01×105Pa时,Vm≠22.4L/mol.
解答 解:A.1molNH4Cl含原6mol原子,个数为6NA,故A错误;
B.10g氖气的物质的量为1mol,所含原子数约为6.02×1023,故B正确;
C.标况下,水是液体,不能使用气体摩尔体积,故C错误;
D.在20℃、1.01×105Pa时,Vm≠22.4L/mol,Vm不确定,无法计算11.2L氮气含有氮原子个数,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确气体摩尔体积使用条件和对象是解题关键,题目难度中等.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
17.下列说法正确的是( )
| A. | 化合物 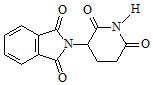 的分子式为C13H9O4N2 的分子式为C13H9O4N2 | |
| B. | CH3(CH2)2CH3与CH(CH3)3具有不同数目的一氯代物 | |
| C. | 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应 | |
| D. | 石油的裂化、裂解属于化学变化,煤的气化、液化则属于物理变化 |
18.在电解水制取H2和O2时,为了增强导电性,常常要加入一些电解质,下列电解质中不适宜加入的是( )
| A. | KNO3 | B. | KI | C. | H2SO4 | D. | Ba(OH)2 |
2.下列物质分类正确的是( )
| A. | Cu(OH)2难溶于水,属于非电解质 | |
| B. | SO2能与碱反应生成盐和水,属于酸性氧化物 | |
| C. | NH4Cl组成中不含金属离子,不属于盐 | |
| D. | HCl气体溶于水电离成H+和Cl-,属于离子化合物 |
19.下列操作过程中实验现象的变化只有一次的是( )
| A. | 石蕊试液中逐滴滴加氯水 | B. | 酚酞试液中加入过氧化钠固体 | ||
| C. | 氢氧化铁胶体中逐滴滴加硫酸 | D. | 碳酸钠溶液中逐滴滴加盐酸 |
16.在澄清透明强酸性溶液中,能大量共存的离子组是( )
| A. | K+、Cu2+、OH-、SO42- | B. | Fe3+、NH4-、NO3-、Cl- | ||
| C. | K+、Na+、Cl-、CO32- | D. | K+、Fe2-、MnO4-、SO42- |
17.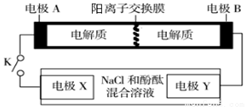 某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
 某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )
某二次电池充、放电的化学方程式为:2K2S2+KI3$?_{充电}^{放电}$ K2S4+3KI.与其它设备连接的电路如图所示.当闭合开关K时,X附近溶液先变红.则下列说法正确的是( )| A. | 放电时,电极A发生还原反应 | |
| B. | A的电极反应式为:3I--2e-=I3- | |
| C. | 当有0.1 mol K+通过离子交换膜,X电极上产生气体1.12 L(标准状况下 | |
| D. | 电池充电时,B电极要与外电源的正极相连,电极上发生还原反应 |