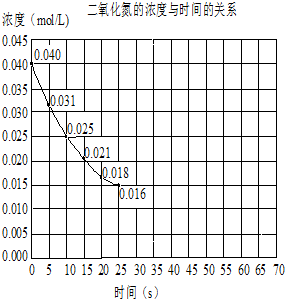
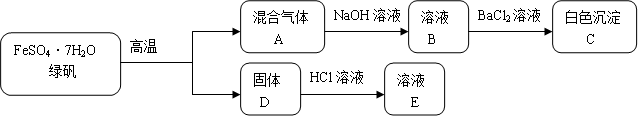
1.用太阳能电解水可获得最理想的单质燃料X,但运输极不方便,国外试用了如下的方法把X转变成便于运输的甲醇燃料;将空气通过极浓的NaOH溶液中,此时空气中的Y有70%被吸收,转变为正盐Z,当Z达到饱和后即加入硫酸,此时溶液会放出纯净的气体Y.一定条件下通过X与Y反应生成甲醇.试回答以下问题:
(1)Z是Na2CO3(写化学式),X和Y反应的化学方程式为CO2+3H2=CH3OH+H2O.
(2)在120℃,如下容积固定的密闭容器中,当活塞被固定在整个装置的中间,X与Y按(1)在Ⅰ中进行反应:
若活塞可左右自由滑动并且导热,起始时Ⅰ中X为n mol,Y为6.5 mol,CH3OH(g)和D各为2 m ol;Ⅱ中A、B、C各为4 mol.当 n 在一定范围内变化时,均可通过调节反应器的温度(Ⅰ和Ⅱ中温度始终相等),使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置.回答下列问题:
①若 n=2.5,则1中起始时反应向正反应(填“正反应”或“逆反应”)方向进行.欲使起始时反应向该方向进行,则 n 的取值范围是1.5<n<4.5.
②若 n 分别取3.0和4.0,则在这两种情况下,当反应分别达到平衡时,A的物质的量不相等(填“相等”或“不相等”),理由是温度不同.
(1)Z是Na2CO3(写化学式),X和Y反应的化学方程式为CO2+3H2=CH3OH+H2O.
(2)在120℃,如下容积固定的密闭容器中,当活塞被固定在整个装置的中间,X与Y按(1)在Ⅰ中进行反应:
| X(g)+Y(g)?CH3OH(g)+D(g) (未配平) | A(g)+B(g)?2C(g) |
①若 n=2.5,则1中起始时反应向正反应(填“正反应”或“逆反应”)方向进行.欲使起始时反应向该方向进行,则 n 的取值范围是1.5<n<4.5.
②若 n 分别取3.0和4.0,则在这两种情况下,当反应分别达到平衡时,A的物质的量不相等(填“相等”或“不相等”),理由是温度不同.
10.动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等.
仪器:①试管,②酒精灯,③烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①③的化学方程式及此实验的结论)
①MgCl2+2H2O=Mg(OH)2↓+H2↑,③2Na+2H2O=2NaOH+H2↑,
此实验的结论:从左到右,同周期元素原子的失电子能力递减,得电子能力递增.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭. |
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等.
仪器:①试管,②酒精灯,③烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①③的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
此实验的结论:从左到右,同周期元素原子的失电子能力递减,得电子能力递增.
8.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
请回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(选填吸热、放热).
(3)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为900℃
(4)900℃时,在1L固定的密闭容器中,加入2mol CO2和1mol H2,反应进行一段时间后,测得CO的浓度为0.5mol/L,则此时该反应是否达到平衡状态否(填“是”或“否”),此时v(正)大于v(逆)(填“大于”“小于”或“等于”),达到平衡时CO2的转化率为33.3%.
(5)化学平衡移动原理同样也适用于溶液中的平衡,已知在氨水中存在下列平衡:
NH3+H2O?NH3•H2O?NH4++OH-
①向氨水中加入MgCl2固体时,平衡向右移动(填“左”或“右”),溶液中OH-的浓度B(填序号,下同),NH4+离子的浓度A.
A.变大B.变小C.不变
②向浓氨水中加入少量的NaOH固体,上述平衡向左移动(填“左”或“右”),溶液中OH-的浓度A(填序号,下同),NH4+离子的浓度B.
A.变大B.变小C.不变.
| t/℃ | 700 | 800 | 900 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.
(2)该反应为吸热反应(选填吸热、放热).
(3)某温度下,平衡浓度符合下式:c(CO2)•c(H2)=c(CO)•c(H2O),试判断此时的温度为900℃
(4)900℃时,在1L固定的密闭容器中,加入2mol CO2和1mol H2,反应进行一段时间后,测得CO的浓度为0.5mol/L,则此时该反应是否达到平衡状态否(填“是”或“否”),此时v(正)大于v(逆)(填“大于”“小于”或“等于”),达到平衡时CO2的转化率为33.3%.
(5)化学平衡移动原理同样也适用于溶液中的平衡,已知在氨水中存在下列平衡:
NH3+H2O?NH3•H2O?NH4++OH-
①向氨水中加入MgCl2固体时,平衡向右移动(填“左”或“右”),溶液中OH-的浓度B(填序号,下同),NH4+离子的浓度A.
A.变大B.变小C.不变
②向浓氨水中加入少量的NaOH固体,上述平衡向左移动(填“左”或“右”),溶液中OH-的浓度A(填序号,下同),NH4+离子的浓度B.
A.变大B.变小C.不变.
6.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1L 1mol/L的盐酸中含HCl分子的数目为NA | |
| B. | 1 mol Cl2与足量的铁反应转移的电子数是3 NA | |
| C. | 常温常压下,15g乙烷分子中含有的共价键键数目为3.5NA | |
| D. | 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA |
5.某原电池装置如图所示,下列有关说法不正确的是( )
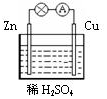

| A. | 锌是该电池的负极 | |
| B. | 锌电极上发生氧化反应 | |
| C. | 铜电极的电极反应式为:2H++2e-=H2↑ | |
| D. | 若将电解质溶液换成AgNO3溶液,两电极的反应式均发生改变 |
4.下列说法正确的是( )
| A. | 在配制一定物质的量浓度溶液的实验中量筒是必需仪器 | |
| B. | 实验室中,盛装NaOH 溶液的试剂瓶用橡皮塞 | |
| C. | 某未知液中加入稀NaOH溶液,没有产生使湿润的红色石蕊试纸变蓝的气体,则该未知液中不含NH4+ | |
| D. | 用pH试纸测定某溶液的pH时,需预先用蒸馏水湿润pH 试纸 |
3.有关硫及其化合物说法正确的是( )
0 160437 160445 160451 160455 160461 160463 160467 160473 160475 160481 160487 160491 160493 160497 160503 160505 160511 160515 160517 160521 160523 160527 160529 160531 160532 160533 160535 160536 160537 160539 160541 160545 160547 160551 160553 160557 160563 160565 160571 160575 160577 160581 160587 160593 160595 160601 160605 160607 160613 160617 160623 160631 203614
| A. | 有浓硫酸参与的反应都是氧化还原反应 | |
| B. | 硫在足量空气中燃烧生成大量SO3 | |
| C. | SO2能使酸性高锰酸钾溶液褪色,体现了漂白性 | |
| D. | 二氧化硫可用于抑制酒类中细菌生长,可在葡萄酒中微量添加 |