题目内容
5.某原电池装置如图所示,下列有关说法不正确的是( )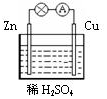
| A. | 锌是该电池的负极 | |
| B. | 锌电极上发生氧化反应 | |
| C. | 铜电极的电极反应式为:2H++2e-=H2↑ | |
| D. | 若将电解质溶液换成AgNO3溶液,两电极的反应式均发生改变 |
分析 该装置中,Zn易失电子发生氧化反应而作负极,铜作正极,正极上氢离子得电子发生还原反应,若将电解质溶液换成AgNO3溶液,正极上银离子得电子发生还原反应,据此分析.
解答 解:A.Zn易失电子发生氧化反应而作负极,故A正确;
B.Zn易失电子发生氧化反应,故B正确;
C.铜作正极,正极上氢离子得电子发生还原反应,铜电极的电极反应式为:2H++2e-=H2↑,故C正确;
D.若将电解质溶液换成AgNO3溶液,正极上银离子得电子发生还原反应,负极上Zn失电子,则负极的反应不变,故D错误;
故选D.
点评 本题考查了原电池原理,根据得失电子的难易程度确定正负极,再结合溶液中得电子的离子来分析解答,题目难度不大.

练习册系列答案
相关题目
16.I.高炉炼铁的主要反应为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.已知该反应的△H<0,在1000℃时,K=64.在1000℃的条件下,在容积10L的密闭容器中,加入Fe、Fe2O3、CO、CO2各1.0moI,反应经10min后达到平衡.
(1)该时间范围内的平均反应速率v(CO2)=0.006mol/(L•min)
(2)CO的转化率60%.
(3)欲提高CO的平衡转化率,可采取的措施是D.
A.减少Fe的量 B.增加Fe2O3的量
C.升高反应温度 D.移出部分CO2
E.使用合适的催化剂 F.减少容器的容积
Ⅱ.已知化学反应:
①Fe(s)+CO2(g)?FeO(s)+CO(g),平衡常数为K1
②Fe(s)+H2O(g)?FeO(s)+H2(g),平衡常数为K2.
在温度973K和1173K情况下,K1、K2的值分别如下:
(4)通过表格中的数值可以推断:反应①的△H> 0.(填“>”“<”)
(5)现有反应③:该反应的平衡常数的数学表达式K3=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$.
(6)根据反应①和②可以推导出K1、K2与K3之间的关系式,K3=$\frac{{K}_{1}}{{K}_{2}}$.据此关系式和上表数据,也能推断出反应③的△H>0(填“>”“<”).
(1)该时间范围内的平均反应速率v(CO2)=0.006mol/(L•min)
(2)CO的转化率60%.
(3)欲提高CO的平衡转化率,可采取的措施是D.
A.减少Fe的量 B.增加Fe2O3的量
C.升高反应温度 D.移出部分CO2
E.使用合适的催化剂 F.减少容器的容积
Ⅱ.已知化学反应:
①Fe(s)+CO2(g)?FeO(s)+CO(g),平衡常数为K1
②Fe(s)+H2O(g)?FeO(s)+H2(g),平衡常数为K2.
在温度973K和1173K情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(5)现有反应③:该反应的平衡常数的数学表达式K3=$\frac{c(CO).c({H}_{2}O)}{c(C{O}_{2}).c({H}_{2})}$.
(6)根据反应①和②可以推导出K1、K2与K3之间的关系式,K3=$\frac{{K}_{1}}{{K}_{2}}$.据此关系式和上表数据,也能推断出反应③的△H>0(填“>”“<”).
13.以二氧化锰为原料制取高锰酸钾晶体的实验流程如图: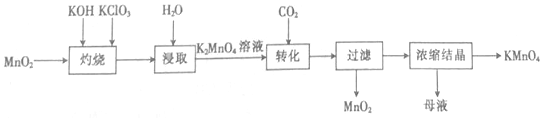
下列有关说法正确的是( )

下列有关说法正确的是( )
| A. | “灼烧”时,可在玻璃坩埚中进行 | |
| B. | “浸取”时,可用无水乙醇代替水 | |
| C. | “转化”反应中,氧化产物与还原产物的物质的量之比为2:1 | |
| D. | “浓缩结晶”后的母液中只有KMnO4和K2CO3两种溶质 |
10.动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等.
仪器:①试管,②酒精灯,③烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①③的化学方程式及此实验的结论)
①MgCl2+2H2O=Mg(OH)2↓+H2↑,③2Na+2H2O=2NaOH+H2↑,
此实验的结论:从左到右,同周期元素原子的失电子能力递减,得电子能力递增.
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭. |
(1)实验目的:研究同周期元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等.
仪器:①试管,②酒精灯,③烧杯,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①③的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
此实验的结论:从左到右,同周期元素原子的失电子能力递减,得电子能力递增.
6. 氨气是一种重要的化工原料,在工农业中都有广泛的应用.
氨气是一种重要的化工原料,在工农业中都有广泛的应用.
(1)NH3和CO2在120℃和催化剂的作用下可以合成尿素,反应方程式为2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).
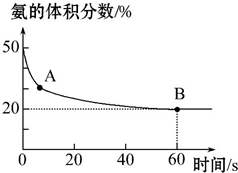
某实验小组向一个容积不变的真空密闭容器中充入CO2与NH3合成尿素,在恒定温度下,混合气体中NH3的体积分数随时间的变化关系如图所示(该条件下尿素为固体).
A点的正反应速率v正(CO2)大于(填“大于”“小于”或“等于”)B点的逆反应速率v逆(CO2),NH3的平衡转化率为75%.
(2)氨基甲酸铵(NH2COONH4)是合成尿素过程的中间产物,现将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:2NH3(g)+CO2(g)?NH2COONH4(s).
实验测得在不同温度下的平衡数据如下表:
①上述反应的焓变:△H<0,熵变△S<0(填“>”“<”或“=”).
②下列说法能说明上述反应建立化学平衡状态的是CD.
A.混合气体的平均相对分子质量不再发生变化
B.混合气体中NH3与CO2的浓度之比不再发生变化
C.混合气体的密度不再发生变化
D.v正(NH3)=2v逆(CO2)
③根据表中数据,列出25.0℃时该反应的化学平衡常数的计算式K=$\frac{1}{(3.2×1{0}^{-3})^{2}×(1.6×1{0}^{-3})}$(不要求计算结果),该反应温度每升高10℃,化学平衡常数就变为原来的2倍.
④温度一定时,向上述容器中再按照NH3和CO2物质的量之比为2:1充入一定量的混合气体,平衡向右(填“向左”“向右”或“不”)移动,该平衡中NH3的浓度与原平衡时NH3浓度相比前者大(填“前者大”“后者大”或“相等”).
 氨气是一种重要的化工原料,在工农业中都有广泛的应用.
氨气是一种重要的化工原料,在工农业中都有广泛的应用.(1)NH3和CO2在120℃和催化剂的作用下可以合成尿素,反应方程式为2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).
某实验小组向一个容积不变的真空密闭容器中充入CO2与NH3合成尿素,在恒定温度下,混合气体中NH3的体积分数随时间的变化关系如图所示(该条件下尿素为固体).
A点的正反应速率v正(CO2)大于(填“大于”“小于”或“等于”)B点的逆反应速率v逆(CO2),NH3的平衡转化率为75%.
(2)氨基甲酸铵(NH2COONH4)是合成尿素过程的中间产物,现将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:2NH3(g)+CO2(g)?NH2COONH4(s).
实验测得在不同温度下的平衡数据如下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (10-3mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.6 |
②下列说法能说明上述反应建立化学平衡状态的是CD.
A.混合气体的平均相对分子质量不再发生变化
B.混合气体中NH3与CO2的浓度之比不再发生变化
C.混合气体的密度不再发生变化
D.v正(NH3)=2v逆(CO2)
③根据表中数据,列出25.0℃时该反应的化学平衡常数的计算式K=$\frac{1}{(3.2×1{0}^{-3})^{2}×(1.6×1{0}^{-3})}$(不要求计算结果),该反应温度每升高10℃,化学平衡常数就变为原来的2倍.
④温度一定时,向上述容器中再按照NH3和CO2物质的量之比为2:1充入一定量的混合气体,平衡向右(填“向左”“向右”或“不”)移动,该平衡中NH3的浓度与原平衡时NH3浓度相比前者大(填“前者大”“后者大”或“相等”).
3.某溶液中可能含有下列6种离子中的某几种:Cl-、SO42-、HCO3-、Na+、K+、Mg2+,所含离子的浓度均相等.为了确认溶液的组成,进行如下实验:取200mL上述溶液,加入足量Ba(OH)2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.88g,向沉淀中加入过量的盐酸,有2.33g.关于原溶液组成的结论,不正确的是( )
| A. | 一定存在SO42-、HCO3-、Mg2+,至少存在Na+、K+中的一种 | |
| B. | 为了确定是否存在Cl-,可向溶液中加入硝酸酸化的硝酸银溶液 | |
| C. | c(HCO3-)=0.05mol/L | |
| D. | 4.88g沉淀中含有3种成分 |
4.下列反应的离子方程式书写正确的是( )
| A. | 铜溶于0.5 mol•L-1的硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| B. | 工业上将Cl2通入石灰乳中制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 向NH4HSO4溶液中滴加少量Ba(OH)2的溶液:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | H2C2O4(弱酸)溶液中加入酸性KMnO4溶液:2MnO42-+5H2C2O4=2Mn2++10CO2↑+2H2O+6OH- |
 如图是一个电化学过程的示意图,请按要求回答下列问题
如图是一个电化学过程的示意图,请按要求回答下列问题