10.下列关于原子核外电子排布规律的说法错误的是( )
| A. | K层是能量最低的电子层 | |
| B. | 原子失电子时先失去能量低的电子 | |
| C. | 核外电子总是优先排布在能量较低的电子层上 | |
| D. | N层为次外层时,最多可容纳的电子数为18 |
9.几种单核微粒具有相同的核电荷数,则这几种微粒( )
| A. | 一定互为同位素 | B. | 一定是同种原子 | ||
| C. | 一定属于同种元素 | D. | 质量数一定相等 |
8.下列排列顺序不正确的是( )
| A. | 元素的非金属性:N<O<F | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 热稳定性:HF>HCl>H2S | D. | 原子半径:Al>Mg>Na |
7.元素R的质量数为A,Rn-的核外电子数为x,则w g Rn-所含中子的物质的量为( )
| A. | (A-x+n) mol | B. | (A-x-n) mol | C. | (A-x+n)$\frac{w}{A}$ mol | D. | (A-x-n)$\frac{w}{A}$ mol |
6.下列叙述正确的是( )
| A. | 化学反应除了生成新的物质外,还伴随着能量的变化 | |
| B. | 物质燃烧不一定是放热反应 | |
| C. | 放热的化学反应不需要加热就能发生 | |
| D. | 吸热反应不加热就不会发生 |
4.对某含铜矿石【主要成分xCuCO3•yCu(OH)2•zCuSiO3,含少量SiO3,FeCO3】进行处理的流程如下:
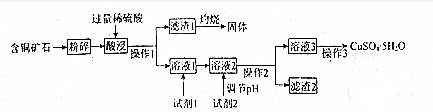
已知:ⅰ.试剂价格:漂液(含25.2%NaClO)450元/吨,双氧水(含30%H2O2)2400元/吨.
ⅱ.溶液中离子浓度小于等于1.0×10-5mol•L-1时,认为该离子沉淀完全.
ⅲ.25℃时,金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表所示,
请回答:
(1)含铜矿石粉碎的目的为增大矿石与稀硫酸的接触面积,加快酸浸速率并使酸浸更充分,滤渣Ⅰ灼烧所得固体的用途为制备光导纤维、制备玻璃、生产硅单质等(任写一种).
(2)操作Ⅰ所用的玻璃仪器为烧杯、漏斗、玻璃棒.
(3)试剂1的名称为漂液,选择该试剂的理由为节约成本,所发生反应的离子方程式为ClO-+2Fe2++2H+=Cl-+2Fe3++H2O.
(4)加入试剂2,需调节溶液的pH的合理范围为3.7≤PH<4.0,试剂2可以选择下列物质中的BC(填选项字母).
A.Cu B.CuO C.Cu(OH)2 D.Fe
(5)操作3包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥、洗涤的方法为用玻璃棒引流向过滤器中加入冷水至浸没沉淀,待水自然流下,重复2-3次.
(6)25℃时,Cu(OH)2 的溶度积常数K溶[Cu(OH)2]=1.0×10-20.

已知:ⅰ.试剂价格:漂液(含25.2%NaClO)450元/吨,双氧水(含30%H2O2)2400元/吨.
ⅱ.溶液中离子浓度小于等于1.0×10-5mol•L-1时,认为该离子沉淀完全.
ⅲ.25℃时,金属离子生成氢氧化物时,开始沉淀和沉淀完全的pH如表所示,
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Cu(OH)2 | 4.0 | 6.5 |
(1)含铜矿石粉碎的目的为增大矿石与稀硫酸的接触面积,加快酸浸速率并使酸浸更充分,滤渣Ⅰ灼烧所得固体的用途为制备光导纤维、制备玻璃、生产硅单质等(任写一种).
(2)操作Ⅰ所用的玻璃仪器为烧杯、漏斗、玻璃棒.
(3)试剂1的名称为漂液,选择该试剂的理由为节约成本,所发生反应的离子方程式为ClO-+2Fe2++2H+=Cl-+2Fe3++H2O.
(4)加入试剂2,需调节溶液的pH的合理范围为3.7≤PH<4.0,试剂2可以选择下列物质中的BC(填选项字母).
A.Cu B.CuO C.Cu(OH)2 D.Fe
(5)操作3包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥、洗涤的方法为用玻璃棒引流向过滤器中加入冷水至浸没沉淀,待水自然流下,重复2-3次.
(6)25℃时,Cu(OH)2 的溶度积常数K溶[Cu(OH)2]=1.0×10-20.
3.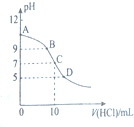 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )| A. | A点溶液中加少量水,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$减小 | |
| B. | 原氨水的物质的量浓度约为1.006×10-2mol•L-1 | |
| C. | B、D两点溶液中水电离出来的c(OH-):B<0 | |
| D. | C点溶液中的H2O不发生电离 |
2.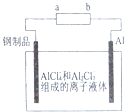 已知:银锌电池放电时总反应为Zn+Ag2O+H2O═Zn(OH)2+2Ag,用银锌电池作电源,在非水体系中完成钢制品上镀铝的原理如图所示,下列说法正确的是( )
已知:银锌电池放电时总反应为Zn+Ag2O+H2O═Zn(OH)2+2Ag,用银锌电池作电源,在非水体系中完成钢制品上镀铝的原理如图所示,下列说法正确的是( )
 已知:银锌电池放电时总反应为Zn+Ag2O+H2O═Zn(OH)2+2Ag,用银锌电池作电源,在非水体系中完成钢制品上镀铝的原理如图所示,下列说法正确的是( )
已知:银锌电池放电时总反应为Zn+Ag2O+H2O═Zn(OH)2+2Ag,用银锌电池作电源,在非水体系中完成钢制品上镀铝的原理如图所示,下列说法正确的是( )| A. | a电极的电极反应式为Ag2O+H2O+2e-=2Ag+2OH- | |
| B. | 银锌电池的电解质溶液可用稀硫酸 | |
| C. | 银锌电池放电时,负极附近溶液的pH增大 | |
| D. | Al电极上发生的电极反应式为Al+7AlCl4--3e-=4Al2Cl4- |
1.短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素同周期,X的金属性再同周期元素中最强,Y原子的电子层数与最外层电子数相等;Z元素在地壳中的含量居于第二位,W的最高价氧化物的水化物的化学式为HnWO2n+2,下列说法正确的是( )
0 155490 155498 155504 155508 155514 155516 155520 155526 155528 155534 155540 155544 155546 155550 155556 155558 155564 155568 155570 155574 155576 155580 155582 155584 155585 155586 155588 155589 155590 155592 155594 155598 155600 155604 155606 155610 155616 155618 155624 155628 155630 155634 155640 155646 155648 155654 155658 155660 155666 155670 155676 155684 203614
| A. | 简单离子半径:X<Y<W | |
| B. | Y、Z两种元素的氧化物均具有两性 | |
| C. | X、W分别形成的氢化物中所含化学键种类相同 | |
| D. | Z、W形成化合物的电子式为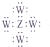 |
