4.某化合物的结构(键线式)及球棍模型如下:
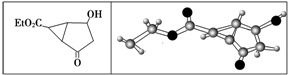
该有机物分子的1H核磁共振谱如下(单位是ppm).
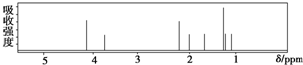
下列关于该有机物的叙述不正确的是( )

该有机物分子的1H核磁共振谱如下(单位是ppm).

下列关于该有机物的叙述不正确的是( )
| A. | 该有机物分子中不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH2CH3 | |
| D. | 该有机物可发生水解反应 |
3.下列各组物质中化学键的类型完全相同的是( )
| A. | NaCl MgCl2 Na2O | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2SO4 | D. | NH4Cl H2O CO2 |
2.六种短周期元素(a、b、c、d、e、f)的原子序数依次增大.其中a与e同主族,b与f同主族,e与f同周期;常温下a、e的单质状态不同;d的核电荷数是b的最外层电子数的2倍;单质f是一种重要的半导体材料.由此可推知( )
| A. | a、c两种元素只能组成化学式为ca3的化合物 | |
| B. | b、c、d分别与a形成的简单化合物,沸点由高到低依次为:d>c>b | |
| C. | 原子半径由大到小的顺序是 e>f>c>b>a | |
| D. | 元素的非金属性由强到弱的顺序是 d>c>f>b |
1.如图所示是四种分子结构的排列方式,其对应的化学式正确的是( )
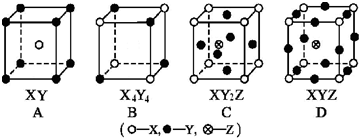

| A. | A | B. | B | C. | C | D. | D |
20.X、Y、Z均为短周期主族元素,其核电荷数依次增大,且它们的原子最外层电子数之比为1:4:2.下列叙述中正确的是( )
| A. | X一定是碱金属元素 | |
| B. | Y元素能形成化合物Na2YO3,且其水溶液呈碱性 | |
| C. | Z元素形成的最高价氧化物熔点较低 | |
| D. | X的单质一定能通过电解Z的盐酸盐溶液制备 |
19.某粒子用${\;}_{Z}^{A}$Rn+表示,下列关于该粒子的叙述中正确的是( )
| A. | 所含质子数=A-n | B. | 所含中子数=A-Z | C. | 所含电子数=A+n | D. | 所含质子数=A+Z |
18.常温下,向20mL 0.5mol•L-1的CH3COOH溶液中逐滴滴加0.5mol•L-1的NaOH溶液,滴定曲线如图.相关分析正确的是( )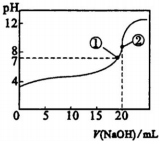

| A. | 滴加至①时,c(Na+)=c(CH3COO-),酸碱恰好完全反应 | |
| B. | 滴加至②时,c(OH-)-c(H+)=c(CH3COOH) | |
| C. | 滴定中,$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$逐渐减小 | |
| D. | 滴定中.c(CH3COOH)与c(CH3 C00-)之和保持不变 |
17.下列说法中正确的是( )
| A. | 共价化合物在熔融态时不能导电 | |
| B. | 氢键是一种化学键,且它比分子间作用力要稍强 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 双原子分子中的共价键一定是非极性键 |
16.在碱性溶液中能大量共存且溶液为无色透明的一组离子是( )
| A. | K+、Na+、Cl-、CO32- | B. | NH4+、Na+、Cl-、SO42- | ||
| C. | Na+、HCO3-、NO3-、SO42- | D. | K+、MnO4-、Na+、Cl- |
15.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
0 154726 154734 154740 154744 154750 154752 154756 154762 154764 154770 154776 154780 154782 154786 154792 154794 154800 154804 154806 154810 154812 154816 154818 154820 154821 154822 154824 154825 154826 154828 154830 154834 154836 154840 154842 154846 154852 154854 154860 154864 154866 154870 154876 154882 154884 154890 154894 154896 154902 154906 154912 154920 203614
| A. | 标准状况下,2.24 L F2所含原子数为0.1NA | |
| B. | 4.4gCO2中氧分子的个数为0.1NA | |
| C. | 78g Na2O2固体中Na+的个数目为NA | |
| D. | 2.3gNa完全燃烧后失去电子的个数为0.1NA |