题目内容
18.常温下,向20mL 0.5mol•L-1的CH3COOH溶液中逐滴滴加0.5mol•L-1的NaOH溶液,滴定曲线如图.相关分析正确的是( )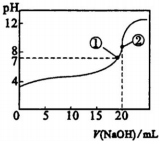
| A. | 滴加至①时,c(Na+)=c(CH3COO-),酸碱恰好完全反应 | |
| B. | 滴加至②时,c(OH-)-c(H+)=c(CH3COOH) | |
| C. | 滴定中,$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$逐渐减小 | |
| D. | 滴定中.c(CH3COOH)与c(CH3 C00-)之和保持不变 |
分析 A.滴加至①时,溶液pH=7,结合电荷守恒:c(H+)+c(Na+)=c(CH3COO-)+c(OH-)判断,若恰好反应,则为醋酸钠溶液,溶液呈碱性,则醋酸稍过量;
B.滴加至②时,此时为醋酸钠溶液,根据质子守恒判断;
C.溶液中存在平衡:CH3COOH?H++CH3COO-,加入氢氧化钠,氢离子被消耗,平衡正向移动;
D.滴定中n(CH3COOH)与n(CH3 COO-)之和保持不变,但溶液体积增大,二者浓度之和会减小.
解答 解:A.滴加至①时,溶液pH=7,则c(H+)=c(OH-),由电荷守恒:c(H+)+c(Na+)=c(CH3COO-)+c(OH-),可知c(Na+)=c(CH3COO-),若恰好反应,则为醋酸钠溶液,溶液呈碱性,则醋酸稍过量,故A错误;
B.滴加至②时,此时为醋酸钠溶液,溶液中氢氧根离子源于水的电离、醋酸根水解,根据质子守恒:c(OH-)=c(H+)+c(CH3COOH),则c(OH-)-c(H+)=c(CH3COOH),故B正确;
C.溶液中存在平衡:CH3COOH?H++CH3COO-,加入氢氧化钠,氢离子被消耗,平衡正向移动,则$\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$增大,故C错误;
D.由物料守恒可知,滴定中n(CH3COOH)与n(CH3 COO-)之和保持不变,但溶液体积增大,二者浓度之和会减小,故D错误.
故选:B.
点评 本题以滴定曲线为载体,考查离子浓度大小比较、弱电解质的电离平衡等,注意理解离子浓度大小比较中物料守恒、电荷守恒、质子恒等式三大守恒应用.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
8.25℃时,在10mL浓度均为0.1mol/L的醋酸和盐酸的混合溶液中,滴加0.1mol/L的NaOH溶液V mL,则溶液中粒子浓度关系正确的是( )
| A. | V=0时:[H+]>[Cl-]=[CH3COOH] | B. | V=10 mL时:[OH-]+[CH3COO-]=[H+] | ||
| C. | V=20 mL时:[Na+]=[CH3COO-]+[Cl-] | D. | 加入NaOH溶液至pH=7时,V>20 mL |
6.下列说法正确的是( )
| A. | 将盐酸和醋酸钠溶液混合后溶液至中性,溶液中c(Na+)=c(Cl-) | |
| B. | 1 mol CH4分子中含有的共价键数目等于1 mol Na2O2固体中含有的离子总数 | |
| C. | 80℃的纯水的pH大于25℃的纯水的pH | |
| D. | 等体积、等pH的盐酸和醋酸与1mol/L的NaOH溶液完全中和,消耗的NaOH溶液体积后者多 |
13.下列关于金属晶体的叙述正确的是( )
| A. | 用铂金做首饰不能用金属键理论解释 | |
| B. | 固态和熔融时易导电,熔点在1 000℃左右的晶体可能是金属晶体 | |
| C. | Li、Na、K的熔点逐渐升高 | |
| D. | 金属导电和熔融电解质(或电解质溶液)导电的原理一样 |
3.下列各组物质中化学键的类型完全相同的是( )
| A. | NaCl MgCl2 Na2O | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2SO4 | D. | NH4Cl H2O CO2 |
10.能说明Cl比S的非金属性强的是( )
①Cl2比S容易与H2化合;
②Cl2能与S2-发生置换反应;
③酸性:HClO3>H2SO3;
④与Fe反应时,Cl2比S得电子数目多;
⑤Cl2比S单质熔、沸点低
⑥酸性:HCl>H2S.
①Cl2比S容易与H2化合;
②Cl2能与S2-发生置换反应;
③酸性:HClO3>H2SO3;
④与Fe反应时,Cl2比S得电子数目多;
⑤Cl2比S单质熔、沸点低
⑥酸性:HCl>H2S.
| A. | 只有④ | B. | ①②④ | C. | ①②③ | D. | ①②③④⑤ |
7.化学与生活密切相关,下列有关说法中不正确的是( )
| A. | 工业上常利用油脂的碱性水解制取肥皂 | |
| B. | 雾、鸡蛋清水溶液、水与乙醇的混合液均具有丁达尔效应 | |
| C. | 蔬菜汁饼干易氧化变质:建议包装饼干时,加入一小包铁粉作抗氧化剂和吸水剂并密封 | |
| D. | 浸泡过高锰酸钾溶液的硅藻士可以吸收乙烯,所以可用此物保鲜水果 |
8.下列反应所得有机产物只有一种的是( )
| A. | 等体积的甲烷与氯气在光照条件下的取代反应 | |
| B. | 丙烯与氯化氢的加成反应 | |
| C. | 2-丙醇在浓硫酸作用下的消去反应 | |
| D. | 乙炔与溴水的加成反应 |
 ;D所在族元素的氢化物中,稳定性最强的是(填化学式)H2O.
;D所在族元素的氢化物中,稳定性最强的是(填化学式)H2O.