题目内容
17.下列说法中正确的是( )| A. | 共价化合物在熔融态时不能导电 | |
| B. | 氢键是一种化学键,且它比分子间作用力要稍强 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 双原子分子中的共价键一定是非极性键 |
分析 A.共价化合物由分子构成;
B.氢键不是化学键;
B.离子化合物中可能含共价键;
C.双原子分子中的共价键,可能为极性键.
解答 解:A.共价化合物由分子构成,熔融不能电离,则不能导电,故A正确;
B.氢键不是化学键,它比分子间作用力要稍强,故B错误;
D.离子化合物中可能含共价键,如NaOH中含O-H共价键,故C错误;
D.双原子分子中的共价键,可能为极性键,如H-Cl为极性键,故D错误;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
相关题目
7.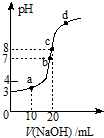 常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )
常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )
 常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )
常温时,用0.10mol/L的NaOH溶液滴定20.00mL 0.10mol/L某 一元酸HA溶液所得滴定曲线如图.下列说法不正确的是( )| A. | a、b、c三点所示溶液导电能力最强的是c点对应的溶液 | |
| B. | 在c点溶液中:c(H+)+c(HA)=c(OH-) | |
| C. | 25℃,HA的电离平衡常数约为1.0×10-5 | |
| D. | a、b、c、d四点所示溶液中水的电离程度最大的是b点对应的溶液 |
8.下列物质与水反应生成强酸的是( )
| A. | Na2O | B. | SO3 | C. | CO2 | D. | NO |
5.下列实验合理的是( )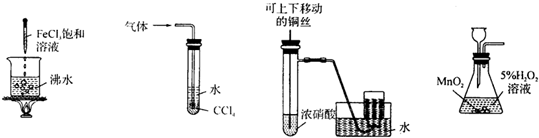

| A. | 得到红褐色沉淀 | B. | 吸收氨气,并防止倒吸 | ||
| C. | 制备并收集少量NO2气体 | D. | 实验室制O2 |
12.25℃某气态烃与氧气混合充入密闭容器中,点火爆炸后,又恢复到25℃,此时容器内压强为开始时的一半,再经氢氧化钠溶液处理,容器内几乎为真空,该烃的分子式为( )
| A. | CH4 | B. | C3H6 | C. | C2H6 | D. | C3H8 |
2.六种短周期元素(a、b、c、d、e、f)的原子序数依次增大.其中a与e同主族,b与f同主族,e与f同周期;常温下a、e的单质状态不同;d的核电荷数是b的最外层电子数的2倍;单质f是一种重要的半导体材料.由此可推知( )
| A. | a、c两种元素只能组成化学式为ca3的化合物 | |
| B. | b、c、d分别与a形成的简单化合物,沸点由高到低依次为:d>c>b | |
| C. | 原子半径由大到小的顺序是 e>f>c>b>a | |
| D. | 元素的非金属性由强到弱的顺序是 d>c>f>b |
9. 甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
 甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )| A. | 丙与戊的原子序数相差26 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丁的最高价氧化物可用于制造光导纤维 |
6.14C常用于测定生物遗骸的年份.下列说法中正确的是( )
| A. | 14C的质量数为14g•mol-1 | B. | 14C与12C是两种不同的元素 | ||
| C. | 14C与C60互为同素异形体 | D. | 14C与14N中子数一定不同 |
