11.某学生用0.1032mol•L-1的盐酸标准溶液滴定未知浓度的KOH溶液,其操作分解为如下几步:
A.取已用蒸馏水洗净的酸式滴定管,用盐酸标准溶液润洗滴定管2~3次;
B.移取20mL待测KOH注入洁净的锥形瓶中,并加入2~3滴甲基橙;
C.取标准盐酸溶液注入酸式滴定管至“0”刻度以上1~2cm;
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
E.调节液面至“0”或“0”以下某一刻度,记录读数;
F.把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点并记录滴定管液面的刻度.
完成下列问题:
(1)上述操作步骤的正确顺序是ACDEBF(填写字母序号).
(2)判断溶液到达滴定终点的方法是当溶液由黄色变为橙色,且在半分钟内不褪色.
(3)上述A步骤操作的目的是滴定管用蒸馏水洗涤后,内壁有一层水膜,如果直接装液会使浓度降低.
(4)若上述B步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果产生的影响是偏高;若称取一定量的KOH固体(含少量NaOH)配制待测溶液并用上述盐酸标准溶液进行滴定,则对滴定结果产生的影响是偏高,理由是因为同质量的NaOH比KOH中和能力强,消耗的盐酸多.
(5)用0.1032mol•L-1的盐酸滴定未知浓度的KOH溶液,重复三次的实验数据如下表所示:
则待测KOH的物质的量浓度是0.1124mol•L-1.
A.取已用蒸馏水洗净的酸式滴定管,用盐酸标准溶液润洗滴定管2~3次;
B.移取20mL待测KOH注入洁净的锥形瓶中,并加入2~3滴甲基橙;
C.取标准盐酸溶液注入酸式滴定管至“0”刻度以上1~2cm;
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液;
E.调节液面至“0”或“0”以下某一刻度,记录读数;
F.把锥形瓶放在滴定管的下面,用标准盐酸滴定至终点并记录滴定管液面的刻度.
完成下列问题:
(1)上述操作步骤的正确顺序是ACDEBF(填写字母序号).
(2)判断溶液到达滴定终点的方法是当溶液由黄色变为橙色,且在半分钟内不褪色.
(3)上述A步骤操作的目的是滴定管用蒸馏水洗涤后,内壁有一层水膜,如果直接装液会使浓度降低.
(4)若上述B步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果产生的影响是偏高;若称取一定量的KOH固体(含少量NaOH)配制待测溶液并用上述盐酸标准溶液进行滴定,则对滴定结果产生的影响是偏高,理由是因为同质量的NaOH比KOH中和能力强,消耗的盐酸多.
(5)用0.1032mol•L-1的盐酸滴定未知浓度的KOH溶液,重复三次的实验数据如下表所示:
| 序号 | 消耗盐酸的体积/mL | 待测KOH溶液的体积/mL |
| 1 | 27.23 | 25.00 |
| 2 | 28.24 | 25.00 |
| 3 | 27.25 | 25.00 |
10. 用中和滴定法测定某烧碱样品的纯度.有以下步骤:
用中和滴定法测定某烧碱样品的纯度.有以下步骤:
(1)配制待测液:用已称好的5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液.除烧杯和玻璃棒外,还需要用到的主要仪器有1000mL容量瓶、胶头滴管.
(2)滴定:
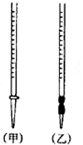
①盛装0.1000mol•L-1的盐酸标准液应该使用甲(选填“甲”或“乙”).
②将一定体积的待测溶液装在锥形瓶内,若采用甲基橙做指示剂,当观察到由橙色变为黄色,且半分钟内不变色时,滴定达到终点.
(3)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①用蒸馏水冲洗锥形瓶后未烘干,测定结果无影响;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外,测定结果偏高;
③读数时,滴定前仰视,滴定后俯视,测定结果偏低.
(4)有关数据记录如下:
根据以上数据计算,烧碱样品的纯度是80.8%.
 用中和滴定法测定某烧碱样品的纯度.有以下步骤:
用中和滴定法测定某烧碱样品的纯度.有以下步骤:(1)配制待测液:用已称好的5.0g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制1000mL溶液.除烧杯和玻璃棒外,还需要用到的主要仪器有1000mL容量瓶、胶头滴管.
(2)滴定:
①盛装0.1000mol•L-1的盐酸标准液应该使用甲(选填“甲”或“乙”).
②将一定体积的待测溶液装在锥形瓶内,若采用甲基橙做指示剂,当观察到由橙色变为黄色,且半分钟内不变色时,滴定达到终点.
(3)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①用蒸馏水冲洗锥形瓶后未烘干,测定结果无影响;
②在滴定过程中不慎将数滴酸液滴在锥形瓶外,测定结果偏高;
③读数时,滴定前仰视,滴定后俯视,测定结果偏低.
(4)有关数据记录如下:
| 测定序号 | 待测溶液的体积(mL) | 所耗盐酸标准液的体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 1 | 20.00 | 0.50 | 20.78 |
| 2 | 20.00 | 1.20 | 21.32 |
| 3 | 20.00 | 0.40 | 21.20 |
8.配置一定物质的量浓度的NaOH溶液时,造成实验结果偏高的是( )
| A. | 定容时俯视液面 | B. | 容量瓶洗净后有少量水残留 | ||
| C. | 转移时没有洗涤烧杯和玻璃 | D. | 所用的氢氧化钠已吸水潮解 |
7.NA代表阿伏加德罗常数的值,以下说法正确的是( )
| A. | 2NA个HCl分子与44.8 L H2和Cl2的混合气体所含的原子数目均为4NA | |
| B. | 32gCu将足量浓、稀硝酸分别还原为NO2和NO,浓、稀硝酸得到的电子数均为NA | |
| C. | 物质的量浓度均为1mol/L的NaCl和MgCl2混合溶液中,含有Cl-的数目为3NA | |
| D. | 1molD3${\;}_{\;}^{18}$O+(其中D代表${\;}_{1}^{2}$H)中含有的中子数为10NA |
6.用氢离子浓度相同的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为V1和V2,则V1和V2的关系正确的是( )
| A. | V1>V2 | B. | V1<V2 | C. | V1=V2 | D. | V1≤V2 |
5.对25℃时的醋酸溶液,若采用下列不同的措施,能使醋酸电离度增大的是( )
| A. | 加入NaOH固体 | B. | 加入醋酸钠晶体 | C. | 加入盐酸 | D. | 降温 |
3.为了增强漂白粉的漂白能力,常在漂白粉溶液中加入少量的( )
| A. | NaOH | B. | NaCl | C. | HCl | D. | Ca(ClO)2 |
2.下列关于氯水的叙述正确的是( )
0 154608 154616 154622 154626 154632 154634 154638 154644 154646 154652 154658 154662 154664 154668 154674 154676 154682 154686 154688 154692 154694 154698 154700 154702 154703 154704 154706 154707 154708 154710 154712 154716 154718 154722 154724 154728 154734 154736 154742 154746 154748 154752 154758 154764 154766 154772 154776 154778 154784 154788 154794 154802 203614
| A. | 新制氯水可使蓝以石蕊试纸先变红,后褪色 | |
| B. | 新制氯水中只含有Cl2和H2O分子 | |
| C. | 氯水放置数天后,酸性增强 | |
| D. | 光照氯水有气泡逸出,该气体是Cl2 |
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: 室温下向10mL 0.1mol•L-1 NaOH溶液中逐滴加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.
室温下向10mL 0.1mol•L-1 NaOH溶液中逐滴加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.