题目内容
4. 室温下向10mL 0.1mol•L-1 NaOH溶液中逐滴加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.
室温下向10mL 0.1mol•L-1 NaOH溶液中逐滴加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.(1)酸碱中和滴定时,用到的仪器有酸式滴定管、碱式滴定管、铁架台(带蝴蝶夹)、锥形瓶.
(2)a点(横坐标为10)所示溶液中,溶质是NaA,溶液中c(Na+)、c(A)、c(H+)、c(OH-)从大到小的顺序为c(Na+)>c(A-)>c(OH-)>c(H+),其中c(Na+)=c(A-)+c(HA)(填“>”“<”或“=”)
(3)c点所示溶液中,c(Na+)=c(A-)(填“>”“<”或“=”)
(4)b点所示溶液中,c(A-)>c(HA)(填“>”“<”或“=”)
(5)a、b、c点所示溶液中,水的电离程度最大的是a.
(6)以下滴定操作会导致V(HA)偏大的是AD.
A、滴定管滴定前有气泡,滴定后气泡消失
B、锥形瓶洗涤后没有干燥
C、滴定时锥形瓶中有液体溅出
D、最后一滴HA溶液附在锥形瓶内壁上未冲下
E、滴定开始前读数时平视,滴定终点,读数时俯视.
分析 (1)中和滴定需要用到铁架台(带蝴蝶夹)、酸式滴定管、碱式滴定管、锥形瓶;
(2)a点时酸碱恰好中和,溶质为NaA,NaA水解呈碱性,溶液中c(Na+)>c(A)>c(OH-)>c(H+);根据物料守恒判断;
(3)c点所示溶液呈中性,根据电荷守恒判断;
(4)b点溶质为等浓度的NaA和HA,HA的电离程度大于NaA的水解程度;
(5)酸或碱抑制水电离,含有弱根离子的盐促进水电离;
(6)根据c(待)=$\frac{c(标)×V(标)}{V(待)}$判断不当操作对V(标)的影响;
解答 解:(1)中和滴定需要用到铁架台(带蝴蝶夹)、酸式滴定管、碱式滴定管、锥形瓶;
故答案为:锥形瓶;
(2)a点时酸碱恰好中和,溶质为NaA,NaA水解呈碱性,A-的水解程度减小,溶液中c(Na+)>c(A)>c(OH-)>c(H+);a点所示溶液中溶质为NaA,根据物料守恒可得:c(Na+)=c(A-)+c(HA);
故答案为:NaA;c(Na+)>c(A-)>c(OH-)>c(H+);=;
(3)c点所示溶液呈中性,则c(OH-)=c(H+),由电荷守恒得:c(Na+)+c(H+)=c(A-)+c(OH-);
所以c(Na+)=c(A-);
故答案为:=;
(4)b点溶质为等浓度的NaA和HA,HA的电离程度大于NaA的水解程度,c(A-)>c(HA);
故答案为:>;
(5)根据图象知,该酸是弱酸,a、b、c点的溶质分别是盐、盐和酸、盐和酸,a点盐类水解促进水电离,b点盐类水解小于酸的电离,水的电离程度受到抑制,c点溶液呈中性,水的电离程度不受影响,所以a、b、c三点溶液中水的电离程度最大的是a;
故答案为:a;
(6)A、滴定管滴定前有气泡,滴定后气泡消失,导致V(HA)偏大,故A正确;
B、锥形瓶洗涤后没有干燥,NaOH的物质的量不变,导致V(HA)不变,故B错误;
C、滴定时锥形瓶中有液体溅出,NaOH的物质的量偏小,导致V(HA)偏小,故C错误;
D、最后一滴HA溶液附在锥形瓶内壁上未冲下,导致V(HA)偏大,故D正确;
E、滴定开始前读数时平视,滴定终点,读数时俯视,导致V(HA)偏小,故E错误;
故选AD.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的分析能力及灵活应用能力.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 称量0.40g NaOH固体,在烧杯中加入100mL 水溶解即可 | |
| B. | 将称量好的固体NaOH放入100 mL容量瓶中,加蒸馏水溶解至环形刻线 | |
| C. | 定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分 | |
| D. | 将烧杯中溶解固体NaOH所得溶液冷却到室温后,转移至容量瓶中 |
①亚硫酸溶液 ②次氯酸钠 ③氯化氢气体 ④蔗糖 ⑤硫酸钡
⑥氨气 ⑦冰醋酸 ⑧硫酸氢钠固体 ⑨氢氧化铁 ⑩NO2
(2)写出下列物质在水中的电离方程式
亚硫酸:H2SO3?H++HSO3-;次氯酸钠:NaClO═ClO-+Na+;
(3)甲、乙两瓶氨水的浓度分别为1mol•L-1、0.1mol•L-1,则c(OH-)甲:c(OH-)乙小于10(填“大于”、“等于”或“小于”).
(4)下表数据均在相同温度下测得,由此可知三种酸的酸性由强到弱的顺序为HZ>HY>HX
| HX | HY | HZ | |
| 浓度 mol•L-1 | 0.1 0.5 | 1.0 1.5 | 2.0 2.5 |
| 电离度 | 0.3% 0.13% | 0.3% 0.24% | 0.5% 0.45% |
①混合气体的颜色不再改变的状态 ②混合气体的密度不再改变的状态
③混合气体的压强不再改变的状态 ④混合气体的平均相对分子质量不再改变的状态
⑤$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)c({O}_{2})}$的比值不再改变的状态.
①c(NH3•H2O)=1×10-3 mol•L-1的氨水b L,
②c(OH-)=1×10-3 mol•L-1的氨水c L,
③c(OH-)=1×10-3 mol•L-1的Ba(OH)2溶液d L.
试判断a、b、c、d的数量大小关系为( )
| A. | a=b>c>d | B. | b>a=d>c | C. | b>a>d>c | D. | c>a=d>b |
| A. | Al3+、Ag+、NO3-、I- | B. | Mg2+、NH4+、NO3-、Cl- | ||
| C. | NH4+、K+、S2-、Br- | D. | Zn2+、Na+、NO3-、SO42- |
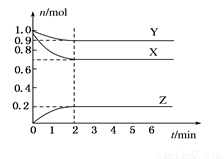
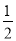 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为____________反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为____________反应(填“放热”或“吸热”)。 2N2O5(g) ΔH<0的影响。
2N2O5(g) ΔH<0的影响。
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: