题目内容
2.下列关于氯水的叙述正确的是( )| A. | 新制氯水可使蓝以石蕊试纸先变红,后褪色 | |
| B. | 新制氯水中只含有Cl2和H2O分子 | |
| C. | 氯水放置数天后,酸性增强 | |
| D. | 光照氯水有气泡逸出,该气体是Cl2 |
分析 氯气与水发生:Cl2+H2O?HCl+HClO,HCl为强酸,完全电离,HClO具有弱酸性部分电离、HClO具有强氧化性、漂白性以及不稳定性,氯水中含有Cl2、HClO和H2O等分子.
解答 解:A.氯气与水发生:Cl2+H2O?HCl+HClO,HCl、HClO电离出的氢离子可使蓝色石蕊试纸先变红,HClO可使蓝色石蕊试纸褪色,故A正确;
B.氯气与水发生:Cl2+H2O?HCl+HClO,HClO为弱酸,氯水中含有Cl2、HClO和H2O等分子,故B错误;
C.HClO不稳定,分解生成HCl,氯水放置数天后,酸性增强,溶液pH减小,故C正确;
D.HClO不稳定,见光分解,发生:2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,生成氧气,故D错误;
故选AC.
点评 本题考查氯水的成分及性质,题目难度不大,注意次氯酸的弱酸性和漂白性.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
7.NA代表阿伏加德罗常数的值,以下说法正确的是( )
| A. | 2NA个HCl分子与44.8 L H2和Cl2的混合气体所含的原子数目均为4NA | |
| B. | 32gCu将足量浓、稀硝酸分别还原为NO2和NO,浓、稀硝酸得到的电子数均为NA | |
| C. | 物质的量浓度均为1mol/L的NaCl和MgCl2混合溶液中,含有Cl-的数目为3NA | |
| D. | 1molD3${\;}_{\;}^{18}$O+(其中D代表${\;}_{1}^{2}$H)中含有的中子数为10NA |
14.室温下,对于0.10mol•L-1的氨水,下列判断正确的是( )
| A. | 其溶液中的c(OH-)=0.1mol•L-1 | |
| B. | 加水稀释后,水电离出的c(OH-)变大 | |
| C. | 加水稀释后,溶液中c(NH4+)•c(OH-)变大 | |
| D. | 与AlCl3溶液发生反应的离子方程式为:Al3++3OH-═Al(OH)3↓ |
11.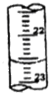 某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液.需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要500mL容量瓶.
(2)滴定:
Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上.
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”刻度线以下,并记录读数.
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液.
Ⅳ.用标准液滴定至终点,记录滴定管液面读数.
①上述滴定步骤中有错误的是(填编号)Ⅰ.该错误操作会导致测定结果偏大(填“偏大”、“偏小”或“无影响”).
②排去碱式滴定管中气泡的方法应采用右图的丙操作.
③步骤Ⅳ中滴定时眼睛应观察锥形瓶中溶液颜色的变化;判断滴定终点的现象是当滴加最后一滴标准液时,待测液由红色刚好变为无色,且半分钟内不变色.
④若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果偏小(填“偏大”、“偏小”或“无影响”)
(3)按正确操作测得有关数据记录如下:按正确操作测得有关数据记录如表:
①a的读数如图所示,则a=22.60; ②烧碱样品的纯度为80.8%
 某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
某学生用0.1000mol/L盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:(1)配制待测液:用2.50g含有少量杂质的固体烧碱样品配制500mL溶液.需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要500mL容量瓶.
(2)滴定:
Ⅰ.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“0”刻度线以上.
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”刻度线以下,并记录读数.
Ⅲ.移取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液.
Ⅳ.用标准液滴定至终点,记录滴定管液面读数.
①上述滴定步骤中有错误的是(填编号)Ⅰ.该错误操作会导致测定结果偏大(填“偏大”、“偏小”或“无影响”).
②排去碱式滴定管中气泡的方法应采用右图的丙操作.
③步骤Ⅳ中滴定时眼睛应观察锥形瓶中溶液颜色的变化;判断滴定终点的现象是当滴加最后一滴标准液时,待测液由红色刚好变为无色,且半分钟内不变色.
④若步骤Ⅱ中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果偏小(填“偏大”、“偏小”或“无影响”)
(3)按正确操作测得有关数据记录如下:按正确操作测得有关数据记录如表:
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |
12.下列实验过程中,始终无明显现象的是( )
| A. | 在稀硫酸中加入铜粉,再加入KNO3固体 | |
| B. | SO2通入Ba(NO3)2溶液中 | |
| C. | CO2通入CaCl2溶液中 | |
| D. | 稀盐酸滴加到Fe(OH)3胶体溶液中 |
 CO2(g)+H2(g)△H<0在427℃时将CO和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状
CO2(g)+H2(g)△H<0在427℃时将CO和H2O(g)各0.01mol通入体积为2升的密闭容器中反应,5分钟时达到平衡状 态,该反应的平衡常数是9,则CO的转化率是多少?(写出计算过程)
态,该反应的平衡常数是9,则CO的转化率是多少?(写出计算过程) 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:(1)该浓硫酸中H2SO4的物质的量浓度为18.4mol/L.
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:(1)该浓硫酸中H2SO4的物质的量浓度为18.4mol/L.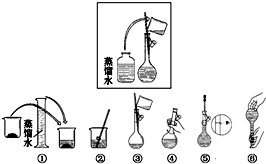 某同学帮助水质检测站配制480mL0.5mol•L-1NaOH溶液.
某同学帮助水质检测站配制480mL0.5mol•L-1NaOH溶液.