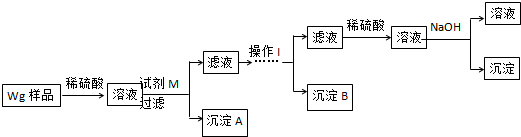
18. 称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
 称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )
称取Na2CO3和NaHCO3混合物样品1.6226g,溶于水配成250.00ml溶液,取出该溶液25.00ml用 0.1mol•L-1 盐酸滴定,得到如图曲线.以下说法错误的是( )| A. | 样品中Na2CO3含量越高,起始pH也越大 | |
| B. | 计量点①中有关离子浓度关系为:c(HCO3-)>C(Cl-)>c(CO32-) | |
| C. | 计量点②溶液中有关离子浓度关系为:2(CO32-)+c(HCO3-)=C(H+)-c(OH-) | |
| D. | 此样品n(NaHCO3)=(28.1-11.9)×10-3mol |
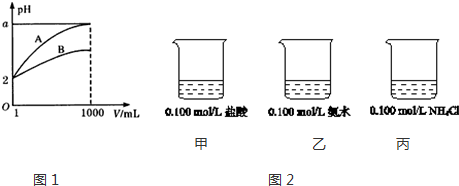
13.下列关于NaOH溶液和氨水的说法正确的是( )
| A. | 相同浓度的两溶液中c(OH-) 相同 | |
| B. | pH=13的两溶液稀释100倍,pH都为11 | |
| C. | 100 mL 0.1 mol/L的两溶液能中和等物质的量的盐酸 | |
| D. | 两溶液中分别加入少量对应的硫酸盐固体,c(OH-) 均明显减小 |
12.下列说法正确的是( )
| A. | 氯水氨水食盐水都能导电,所以Cl2、NH3和氯化钠都是电解质 | |
| B. | 向醋酸溶液中加入少量醋酸溶液,原醋酸电离平衡一定向正向移动 | |
| C. | 升高温度能促进弱电解质的电离 | |
| D. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
10. 常温下有下列四种溶液:
常温下有下列四种溶液:
已知该温度下醋酸的电离平衡常数Ka=1.8×10-5.
请回答下列问题:
(1)用④的标准液滴定③宜选用酚酞(填“石蕊”、“酚酞”或“四基橙”)作为指示剂,①和②两种溶液中由水电离出的c(H+)之比为106:1,
(2)都是0.1mol/L的①NH4Cl②NH4HCO3③CH3COONH4 ④NH4HSO4的溶液中NH4+离子浓度大小顺序为④>①>③>②.(用序号填空)
(3)取溶液③滴定20mL溶液④,滴定曲线如图所示,则a点时溶液中各离子浓度的大小关系为c(Na+)>c(OH-)>c(CH3COO-)>c(H+);若b点时消耗③的体积为V mL,则V>20(填“>”、“<”或“=”).
0 154573 154581 154587 154591 154597 154599 154603 154609 154611 154617 154623 154627 154629 154633 154639 154641 154647 154651 154653 154657 154659 154663 154665 154667 154668 154669 154671 154672 154673 154675 154677 154681 154683 154687 154689 154693 154699 154701 154707 154711 154713 154717 154723 154729 154731 154737 154741 154743 154749 154753 154759 154767 203614
 常温下有下列四种溶液:
常温下有下列四种溶液:| 序号 | ① | ② | ③ | ④ |
| 溶液 | pH=4的NH4Cl溶液 | pH=4的盐酸 | 0.1mol•L-1的醋酸溶液 | 0.1mol•L-1的NaOH溶液 |
请回答下列问题:
(1)用④的标准液滴定③宜选用酚酞(填“石蕊”、“酚酞”或“四基橙”)作为指示剂,①和②两种溶液中由水电离出的c(H+)之比为106:1,
(2)都是0.1mol/L的①NH4Cl②NH4HCO3③CH3COONH4 ④NH4HSO4的溶液中NH4+离子浓度大小顺序为④>①>③>②.(用序号填空)
(3)取溶液③滴定20mL溶液④,滴定曲线如图所示,则a点时溶液中各离子浓度的大小关系为c(Na+)>c(OH-)>c(CH3COO-)>c(H+);若b点时消耗③的体积为V mL,则V>20(填“>”、“<”或“=”).
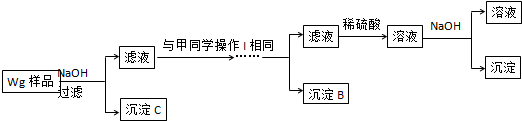
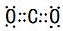 .
.