题目内容
17.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有SiO2、Al2O3、Fe2O3等杂质.以铬铁矿为原料制备重铬酸钾(K2Cr2O7)、重铬酸钠(Na2Cr2O7)的过程如下图所示.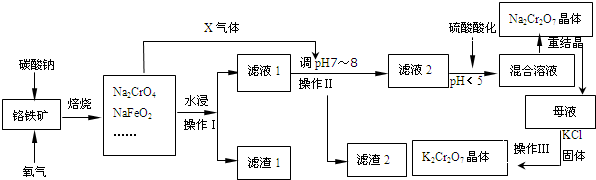
已知:①NaFeO2遇水强烈水解:NaFeO2+2H2O═NaOH+Fe(OH)3↓;
②Cr2O72-+H2O?2CrO42-+2H+.
请回答:
(1)“焙烧”后的固体产物成分除Na2CrO4、NaFeO2外,还有NaAlO2、Na2SiO3(填化学式)
等.写出“焙烧”过程中所发生的氧化还原反应的化学方程式4FeO•Cr2O3+7O2+10Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+4NaFeO2+10CO2.
(2)“焙烧”过程中,所产生X气体的电子式为
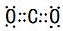 .
.(3)“水浸”步骤中,为了提高浸出率,可采取的措施有(请写出两条):加热、搅拌、研磨或延长浸出时间等;
(4)滤渣1的主要成分是Fe(OH)3.若要进一步分离滤渣2 中的可酸溶成分,请写出酸溶时发生反应的离子方程式Al(OH)3+3H+=Al3++H2O.
(5)含Na2Cr2O7的“混合溶液”经过蒸发并冷却至30~40℃得到的Na2Cr2O7晶体还要进行重结晶,其目的是进一步减少晶体中杂质Na2SO4(填化学式)的含量.
(6)操作Ⅲ由多步组成,向含Na2Cr2O7的母液中加入KCl固体,最终获得K2Cr2O7晶体的操作依次是蒸发浓缩、冷却结晶、过滤、75%乙醇水溶液洗涤、干燥.
分析 铬铁矿的主要成分可表示为FeO•Cr2O3,还含有SiO2、Al2O3、Fe2O3等杂质,将铬铁矿和碳酸钠、氧气混合焙烧,发生反应4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2、Na2CO3+Al2O3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑、Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑、Na2CO3+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2NaFeO2+CO2↑,根据方程式知,生成的气体X是二氧化碳;
然后水浸时发生NaFeO2+2H2O=NaOH+Fe(OH)3↓,过滤得到滤渣1和滤液1,根据信息①知,滤液1中主要是NaAlO2、Na2SiO3、Na2CrO4、NaOH,滤渣1为Fe(OH)3;将滤液1通入X气体,CO2与NaAlO2、Na2SiO3反应生成H2SiO3、Al(OH)3,滤渣2是H2SiO3、Al (OH)3,滤液2主要是Na2CrO4,加入硫酸酸化,溶质变为Na2Cr2O7,将混合溶液蒸发浓缩、冷却结晶得到Na2Cr2O7晶体,将晶体溶于母液,然后加入KCl固体,因为Na2Cr2O7的溶解度大于K2Cr2O7,所以得到K2Cr2O7晶体,采用过滤方法得到K2Cr2O7晶体,
(1)根据发生的反应确定固体产物成分;FeO•Cr2O3和氧气发生氧化还原反应;
(2)通过以上分析知,X是二氧化碳,二氧化碳是共价化合物,每个O原子和C原子形成2对共用电子对;
(3)增大反应速率的方法有:升高温度、增大反应物接触面积等;
(4)结合题给信息确定滤渣成分;氢氧化铝易溶于强酸、强碱溶液;
(5)得到的溶液中溶质还有硫酸钠;
(6)从溶液中获取溶质,需要蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
解答 解:铬铁矿的主要成分可表示为FeO•Cr2O3,还含有SiO2、Al2O3、Fe2O3等杂质,将铬铁矿和碳酸钠、氧气混合焙烧,发生反应4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2、Na2CO3+Al2O3$\frac{\underline{\;高温\;}}{\;}$2NaAlO2+CO2↑、Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑、Na2CO3+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2NaFeO2+CO2↑,根据方程式知,生成的气体X是二氧化碳;
然后水浸时发生NaFeO2+2H2O=NaOH+Fe(OH)3↓,过滤得到滤渣1和滤液1,根据信息①知,滤液1中主要是NaAlO2、Na2SiO3、Na2CrO4、NaOH,滤渣1为Fe(OH)3;将滤液1通入X气体,CO2与NaAlO2、Na2SiO3反应生成H2SiO3、Al(OH)3,滤渣2是H2SiO3、Al (OH)3,滤液2主要是Na2CrO4,加入硫酸酸化,溶质变为Na2Cr2O7,将混合溶液蒸发浓缩、冷却结晶得到Na2Cr2O7晶体,将晶体溶于母液,然后加入KCl固体,因为Na2Cr2O7的溶解度大于K2Cr2O7,所以得到K2Cr2O7晶体,采用过滤方法得到K2Cr2O7晶体,
(1)通过以上分析知,“焙烧”后的固体产物成分除Na2CrO4、NaFeO2外,还有NaAlO2、Na2SiO3;焙烧过程中发生的氧化还原反应为4FeO•Cr2O3+7O2+10Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+4NaFeO2+10CO2,
故答案为:NaAlO2、Na2SiO3;4FeO•Cr2O3+7O2+10Na2CO3$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+4NaFeO2+10CO2;
(2)通过以上分析知,生成的气体是二氧化碳,其电子式为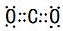 ,故答案为:
,故答案为: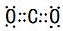 ;
;
(3)“水浸”步骤中,为了提高浸出率,可采取的措施有加热、搅拌、研磨或延长浸出时间等,
故答案为:加热、搅拌、研磨或延长浸出时间等;
(4)通过以上分析知,滤渣1的主要成分是Fe(OH)3;滤渣2是H2SiO3、Al (OH)3,酸溶时发生反应的离子方程式为:Al(OH)3+3H+=Al3++H2O,
故答案为:Fe(OH)3 ;Al(OH)3+3H+=Al3++H2O;
(5)含Na2Cr2O7的“混合溶液”经过蒸发并冷却至30~40℃得到的Na2Cr2O7晶体还要进行重结晶,其目的是进一步减少晶体中杂质Na2SO4的含量,
故答案为:Na2SO4;
(6)从溶液中获取晶体的方法是蒸发浓缩、冷却结晶,故答案为:蒸发浓缩;冷却结晶.
点评 本题考查物质的制备实验及混合物的分离和提纯,为高频考点,把握流程图中每一步发生的反应及操作方法是解本题关键,注意结合题给信息解答,侧重分析与实验能力的考查,题目难度中等.

| A. | 某芳香烃的分子式为C10H14,不能使溴水因反应而褪色,苯环上只有一个取代基,符合条件的烃有4种 | |
| B. | 按照系统命名法,有机物 的命名为2,2,4,4,5-五甲基-3,3-二乙基己烷 的命名为2,2,4,4,5-五甲基-3,3-二乙基己烷 | |
| C. | 甲烷、甲醛、甲酸甲脂都不存在同分异构体 | |
| D. | 某有机物含有C、H、O、N四种元素,其球棍模型为 该有机物能发生取代反应 该有机物能发生取代反应 |
| A. | 1 mol•L-1的氨水溶液中c(OH-)=0.01 mol•L-1 | |
| B. | 常温下,将pH为12的氨水溶液加水稀释100倍,稀释后的溶液pH大于10 | |
| C. | 10 mL 1 mol•L-1的氨水溶液恰好与10 mL 1 mol•L-1的盐酸完全反应 | |
| D. | 在相同条件下,氨水溶液的导电性比NaOH溶液弱 |
| A. | 氯水氨水食盐水都能导电,所以Cl2、NH3和氯化钠都是电解质 | |
| B. | 向醋酸溶液中加入少量醋酸溶液,原醋酸电离平衡一定向正向移动 | |
| C. | 升高温度能促进弱电解质的电离 | |
| D. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
| A. | 该温度下,0.0l mol/L醋酸溶液的pH=4 | |
| B. | 该温度下,用0.1 mol/L醋酸和0.01 mol/L醋酸分别完全中和等体积0.1 mol/L的NaOH溶液,消耗两醋酸的体积比为1:10 | |
| C. | 该温度下,0.2 mol/L醋酸溶液和0.4 mol/L醋酸钠溶液等体积混合后,混合液的pH<4.7 | |
| D. | 该温度下,0.2 mol/L盐酸溶液和0.4 mol/L醋酸钠溶液等体积混合后,混合液的pH>4.7 |
| A. | 常温常压下,14 g丙烯和丁烯的混合气体含有的原子数为6NA | |
| B. | 25℃,pH=1的1 L H2SO4溶液含有的H+数目为0.2NA | |
| C. | 1 mol Fe与一定量的HNO3反应,转移的电子数目一定为3NA | |
| D. | 标准状况下,22.4 L NO和O2的混合气体中所含原子数为2NA |
| A. | ②④ | B. | ①②④ | C. | ②③ | D. | ①④⑤ |