9.下列有关叙述正确的是( )
| A. | NH3•H2O的电离平衡常数随着温度升高而减小 | |
| B. | 在0.10 mol•L-1CH3COOH溶液中,加入少量CH3COONa晶体后,溶液的pH减小 | |
| C. | 强酸、强碱和大部分盐类都是强电解质,其他化合物都是弱电解质 | |
| D. | 相同温度下,醋酸溶液的导电能力可能比稀硫酸强 |
8.氨水的下列性质中,不能证明它是弱电解质的是( )
| A. | 1 mol•L-1的氨水溶液中c(OH-)=0.01 mol•L-1 | |
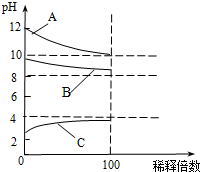
| B. | 常温下,将pH为12的氨水溶液加水稀释100倍,稀释后的溶液pH大于10 | |
| C. | 10 mL 1 mol•L-1的氨水溶液恰好与10 mL 1 mol•L-1的盐酸完全反应 | |
| D. | 在相同条件下,氨水溶液的导电性比NaOH溶液弱 |
7.已知 25℃时有关弱酸的电离平衡常数:则下列说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
| A. | 等物质的量浓度的各溶液 pH 关系为:pH ( NaCN)>pH(Na2CO3)>pH( CH3COONa) | |
| B. | 浓度均为0.2mol/L NaHCO3和 Na2CO3溶液中,存在的粒子种类不相同 | |
| C. | 0.4 mol•L-1HCN 溶液与 0.2 mol•L-1NaOH 溶液等体积混合后,所得溶液中:c(Na+)>c(OH-)>c(H+) | |
| D. | 25℃时,pH=4且浓度均为0.1 mol•L-1的 CH3COOH、CH3COONa混合溶液中:c(Na+)+c(H+)>c(CH3COO-)+c(CH3COOH) |
6.下列叙述中,能说明乙酸的酸性比碳酸强的是( )
| A. | 乙酸具有挥发性 | B. | 乙酸是一元酸 | ||
| C. | 乙酸是有机酸而碳酸是无机酸 | D. | 乙酸能与碳酸氢钠反应放出CO2 |
5.室温下向10mL pH=3的醋酸溶液中加入水稀释10倍后,下列说法正确的是( )
| A. | 溶液中导电粒子的数目增加,导电性增强 | |
| B. | 醋酸的电离程度增大,c(H+)减小 | |
| C. | 再加入10mL pH=11 NaOH溶液,混合液pH=7 | |
| D. | 稀释后溶液pH=4 |
4.已知25℃时有关弱酸的电离平衡常数:则下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A. | 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| B. | a mol•L-1 HCN溶液与b mol•L-1 NaOH溶液等体积混合后,若所得溶液中c(Na+)>c(CN-),则a可能大于b | |
| C. | 冰醋酸中逐滴加水,则溶液的导电性、醋酸的电离度均先增大后减小 | |
| D. | NaHCO3溶液中,一定存在c(Na+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
2.下列说法正确的是( )
0 154570 154578 154584 154588 154594 154596 154600 154606 154608 154614 154620 154624 154626 154630 154636 154638 154644 154648 154650 154654 154656 154660 154662 154664 154665 154666 154668 154669 154670 154672 154674 154678 154680 154684 154686 154690 154696 154698 154704 154708 154710 154714 154720 154726 154728 154734 154738 154740 154746 154750 154756 154764 203614
| A. | 由0.1 mol/L一元碱BOH溶液的pH=10,可推知溶液存在BOH=B++OH- | |
| B. | 醋酸溶于水并达到电离平衡后,加水稀释,则溶液中的c(OH-)减小 | |
| C. | pH=3的醋酸加水稀释后,CH3COOH电离程度增大,醋酸电离常数不变 | |
| D. | 醋酸在醋酸钠溶液中的电离程度大于纯水中的电离程度 |
 现有常温时浓度相同的五种电解质溶液:①CH3COOH ②Na2CO3 ③HNO3④CH3COONa ⑤NaOH
现有常温时浓度相同的五种电解质溶液:①CH3COOH ②Na2CO3 ③HNO3④CH3COONa ⑤NaOH