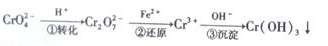3.如图所示,装置在常温下工作(溶液体积变化忽略不计).闭合K,灯泡发光.下列叙述中不正确的是( )
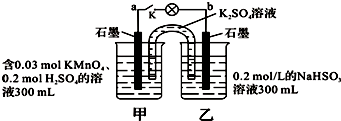

| A. | 当电路中有1.204×1022个电子转移时,乙烧杯中溶液的C(H+)约为0.1 mol•L-1 | |
| B. | 电池工作时,盐桥中的K+移向甲烧杯 | |
| C. | 电池工作时,外电路的电子方向是从a到b | |
| D. | 乙池中的氧化产物为SO42- |
2. 固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,
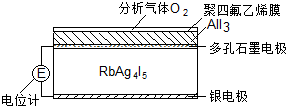
室温导电率达0.27Ω-1•cm-1.利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图.被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量.在气体传感器工作过程中,下列变化肯定没有发生的是( )
 固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体.这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体.目前固体电解质在制造全固态电池及
其它传感器、探测器等方面的应用日益广泛.如RbAg4I5晶体,其中迁移的离子全是Ag+,
室温导电率达0.27Ω-1•cm-1.利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图.被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量.在气体传感器工作过程中,下列变化肯定没有发生的是( )
| A. | 4AlI3+3O2=2Al2O3+6I2 | B. | I2+2Ag++2e-=2AgI | ||
| C. | Ag-e-=Ag+ | D. | I2+2Rb++2e-=2RbI |
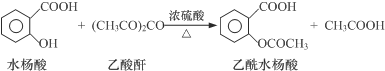
1.工业上常用水杨酸与乙酸酐反应制取解热镇痛药阿司匹林(乙酰水杨酸).
【反应原理】
【物质性质】
【实验流程】
(1)物质制备:向125mL的锥形瓶中依次加入4g水杨酸、10mL乙酸酐(密度为1.08g/mL)、0.5mL浓硫酸,振荡锥形瓶至水杨酸全部溶解,在85℃~90℃条件下,用热水浴加热5~10min.
①加入水杨酸、乙酸酐后,需缓慢滴加浓硫酸,否则产率会大大降低,其原因是水杨酸属于酚类物质,会被浓H2SO4氧化.
②控制反应温度85℃~90℃的原因既保证有较高的反应速率又减少了物质的挥发.
(2)产品结晶:取出锥形瓶,加入50mL蒸馏水冷却.待晶体完全析出后用布氏漏斗抽滤,再洗涤晶体,抽干.简要叙述如何洗涤布氏漏斗中的晶体?向布氏漏斗中加入冰水至浸没所有晶体,重复2~3次.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂X并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸3.6g.
①试剂X为饱和碳酸钠溶液.
②实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色,其可能的原因是产品中仍然可能含有水杨酸.
【反应原理】

【物质性质】
| 试剂 | 沸点(℃) | 溶解度 | 化学性质 |
| 水杨酸 | 211 | 微溶于冷水,易溶于热水 | |
| 乙酸酐 | 139 | 在水中逐渐分解 | |
| 乙酰水杨酸 | 微溶于水 | 与碳酸钠反应生成水溶性盐 |
(1)物质制备:向125mL的锥形瓶中依次加入4g水杨酸、10mL乙酸酐(密度为1.08g/mL)、0.5mL浓硫酸,振荡锥形瓶至水杨酸全部溶解,在85℃~90℃条件下,用热水浴加热5~10min.
①加入水杨酸、乙酸酐后,需缓慢滴加浓硫酸,否则产率会大大降低,其原因是水杨酸属于酚类物质,会被浓H2SO4氧化.
②控制反应温度85℃~90℃的原因既保证有较高的反应速率又减少了物质的挥发.
(2)产品结晶:取出锥形瓶,加入50mL蒸馏水冷却.待晶体完全析出后用布氏漏斗抽滤,再洗涤晶体,抽干.简要叙述如何洗涤布氏漏斗中的晶体?向布氏漏斗中加入冰水至浸没所有晶体,重复2~3次.
(3)产品提纯:将粗产品转移至150mL烧杯中,向其中慢慢加入试剂X并不断搅拌至不再产生气泡为止.进一步提纯最终获得乙酰水杨酸3.6g.
①试剂X为饱和碳酸钠溶液.
②实验中乙酰水杨酸的产率为69%(已知:水杨酸、乙酰水杨酸的相对分子质量分别为138和180).
(4)纯度检验:取少许产品加入盛有5mL水的试管中,加入1~2滴FeCl3溶液,溶液呈浅紫色,其可能的原因是产品中仍然可能含有水杨酸.
20.用O2将HCl转化为Cl2,反应方程式为:4HCl(g)+O2(g)?2H2O(g)+2Cl2(g)+Q(Q>0)
一定条件下测得反应过程中n(Cl2)的实验数据如下.下列说法正确的是( )
一定条件下测得反应过程中n(Cl2)的实验数据如下.下列说法正确的是( )
| t/min | 0 | 2 | 4 | 6 |
| n(Cl2)/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
| A. | 0~2 min的反应速率小于4~6 min的反应速率 | |
| B. | 2~6 min用Cl2表示的反应速率为0.9 mol/(L•min) | |
| C. | 增大压强可以提高HCl转化率 | |
| D. | 平衡常数K(200℃)<K(400℃) |
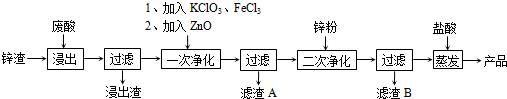
19.工业废弃物对环境的危害极大,硫酸工业废渣废弃物的主要成分为MgO、Al2O3、Fe2O3、SiO2.某同学设计以下方案,变废为宝提取废渣中的金属元素.
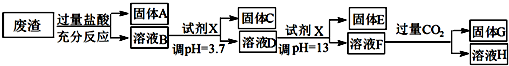
已知常温条件下:
①阳离子以氢氧化物形式完全沉淀(阳离子浓度低于10?5mol•L-1)时溶液的pH:
②饱和氨水溶液中c(OH-)约为1×10-3mol•L-1.
请回答:
(1)写出A与氢氟酸反应的化学方程式:SiO2+4HF=SiF4↑+2H2O.
(2)上述流程中两次使用试剂X,推测试剂X是氢氧化钠(填“氨水”或“氢氧化钠”)其理由是经过计算饱和氨水的pH=11,使用氨水不能将溶液调至pH=13,所以选择氢氧化钠调节溶液酸碱性.
(3)写出F→H的反应离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是镁离子沉淀不完全或氢氧化铝溶解不完全.
(5)固体C跟HI反应的离子方程式为:2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O.
(6)试计算Mg(OH)2的Ksp=10-11.

已知常温条件下:
①阳离子以氢氧化物形式完全沉淀(阳离子浓度低于10?5mol•L-1)时溶液的pH:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| pH | 3.4 | 5.2 | 11 |
请回答:
(1)写出A与氢氟酸反应的化学方程式:SiO2+4HF=SiF4↑+2H2O.
(2)上述流程中两次使用试剂X,推测试剂X是氢氧化钠(填“氨水”或“氢氧化钠”)其理由是经过计算饱和氨水的pH=11,使用氨水不能将溶液调至pH=13,所以选择氢氧化钠调节溶液酸碱性.
(3)写出F→H的反应离子方程式:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)溶液D到固体E过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是镁离子沉淀不完全或氢氧化铝溶解不完全.
(5)固体C跟HI反应的离子方程式为:2Fe(OH)3+2I-+6H+=2Fe2++I2+6H2O.
(6)试计算Mg(OH)2的Ksp=10-11.
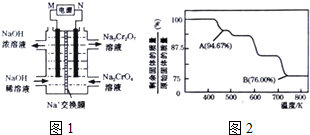
16.用电解法可提纯含有某些含氧酸根杂质的粗KOH溶液,其工作原理如图所示.下列有关说法错误的是
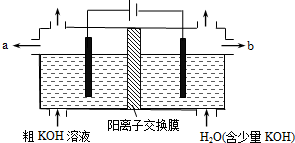 ( )
( )
0 154181 154189 154195 154199 154205 154207 154211 154217 154219 154225 154231 154235 154237 154241 154247 154249 154255 154259 154261 154265 154267 154271 154273 154275 154276 154277 154279 154280 154281 154283 154285 154289 154291 154295 154297 154301 154307 154309 154315 154319 154321 154325 154331 154337 154339 154345 154349 154351 154357 154361 154367 154375 203614
 ( )
( )| A. | 阳极反应式为4OH--4e-=2H2O+O2↑ | B. | 通电后阴极区附近溶液pH会增大 | ||
| C. | K+通过交换膜从阴极区移向阳极区 | D. | 纯净的KOH溶液从b出口导出 |
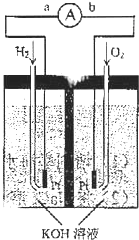 氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,附气体的能力强,性质稳定,请回答: