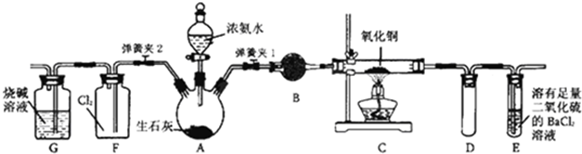
4.下列有关物质性质和用途的描述,正确的是( )
| A. | 氢氟酸具有强酸性,可用于雕刻玻璃 | |
| B. | 浓硫酸具有吸水性,可用浓硫酸干燥SO2、H2S、NO2等气体 | |
| C. | 常温下,铝比铁耐腐蚀,可用铝锅长期盛放酸性食物 | |
| D. | 氨气与氯气能反应生成氯化铵,可用浓氨水检验输送氯气的管道是否有泄漏 |
3.下列实验操作和数据记录都正确的是( )
| A. | 用托盘天平称量时,将NaOH固体放在右盘内的纸上,称得质量为10.2g | |
| B. | 用25mL碱式滴定管量取高锰酸钾溶液,体积为16.60mL | |
| C. | 用干燥的广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10mL量筒量取NaCl溶液,体积为9.2mL |
2.下列关于离子浓度的说法正确的是( )
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值减小 | |
| B. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)>c(CH3COO -) | |
| C. | 常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| D. | c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c(NH4)2SO4>c(NH4Cl) |
20.下列有关说法正确的是( )
| A. | 根据HA、HB的电离常数的相对大小可以直接判断两种溶液的酸性强弱 | |
| B. | 常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 | |
| C. | 加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 | |
| D. | 将浓硫酸和浓硝酸混合后立即放入铁片,铁片被钝化的效果一定会更好 |
19.已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O?CH3COO-+H3O+K1=1.75×10-5 mol•L-1
CH3COO-+H2O?CH3COOH+OH-K2=5.71×10-10 mol•L-1
现将 50mL 0.2mol•L-1 醋酸与 50mL 0.2mol•L-1 醋酸钠溶液混合制得溶液甲,下列叙 述正确的是( )
CH3COOH+H2O?CH3COO-+H3O+K1=1.75×10-5 mol•L-1
CH3COO-+H2O?CH3COOH+OH-K2=5.71×10-10 mol•L-1
现将 50mL 0.2mol•L-1 醋酸与 50mL 0.2mol•L-1 醋酸钠溶液混合制得溶液甲,下列叙 述正确的是( )
| A. | 溶液甲的 pH>7 | |
| B. | 对溶液甲进行微热,K1、K2 同时增大 | |
| C. | 若在溶液甲中加入少量的 NaOH 溶液,溶液的 pH 明显增大 | |
| D. | 若在溶液甲中加入 5 mL 0.1 mol•L-1 的盐酸,则溶液中醋酸的 K1 会变大 |
18.从柑橘中可提炼出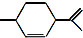 下列关于它的说法不正确的是( )
下列关于它的说法不正确的是( )
 下列关于它的说法不正确的是( )
下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | B. | 其一氯代物有8种 | ||
| C. | 能与溴水发生加成反应 | D. | 常温下呈液态,难溶于水 |
17.在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.25mol/L,向其中加入 1.92g铜粉,微热,充分反应后溶液中c(NO3-)约为( )
| A. | 0.15mol/L | B. | 0.20mol/L | C. | 0.225mol/L | D. | 0.30mol/L |
16.正在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关Fe2O3及硫酸盐的信息,以证明火星上存在或曾经存在过H2O.以下叙述正确的是( )
| A. | 硫酸盐都易溶于水 | |
| B. | 检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品-→粉碎-→加水溶解-→过滤-→向滤液中滴加KSCN溶液 | |
| C. | 分别还原a mol Fe2O3所需H2、Al、CO物质的量之比为3:2:3 | |
| D. | 明矾含有结晶水,是混合物 |
15. (1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
(1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
浓度均为0.1mol•L-1的下列5种溶液:
①CH3COONH4 ②CH3COONa ③NaNO2 ④HF ⑤NH4Cl,
溶液pH值由小到大的顺序是(填写编号)④⑤①③②.
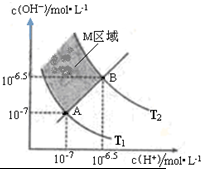
(2)如图表示某溶液中c(H+)和c(OH-)的关系,下列判断正确的是AC.
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.AB线上任意点均有pH=7
C.图中T1<T2
D.M区域内(阴暗部分)任意点均有c(H+)>c(OH-)
0 154161 154169 154175 154179 154185 154187 154191 154197 154199 154205 154211 154215 154217 154221 154227 154229 154235 154239 154241 154245 154247 154251 154253 154255 154256 154257 154259 154260 154261 154263 154265 154269 154271 154275 154277 154281 154287 154289 154295 154299 154301 154305 154311 154317 154319 154325 154329 154331 154337 154341 154347 154355 203614
 (1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
(1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:| 电解质 | HF | CH3COOH | HNO2 | NH3•H2O |
| 电离平衡常数K | 3.53×10-4 | 1.76×10-5 | 4.6×10-4 | 1.77×10-5 |
①CH3COONH4 ②CH3COONa ③NaNO2 ④HF ⑤NH4Cl,
溶液pH值由小到大的顺序是(填写编号)④⑤①③②.
(2)如图表示某溶液中c(H+)和c(OH-)的关系,下列判断正确的是AC.
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.AB线上任意点均有pH=7
C.图中T1<T2
D.M区域内(阴暗部分)任意点均有c(H+)>c(OH-)