题目内容
17.在100mL某混合溶液中,c(HNO3)=0.4mol/L,c(H2SO4)=0.25mol/L,向其中加入 1.92g铜粉,微热,充分反应后溶液中c(NO3-)约为( )| A. | 0.15mol/L | B. | 0.20mol/L | C. | 0.225mol/L | D. | 0.30mol/L |
分析 100mL混合液中显示的物质的量为:n(HNO3)=0.1L×0.4mol/L=0.04mol,含有硫酸的物质的量为:n(H2SO4)=0.1L×0.25moL/L=0.025moL,溶液中氢离子浓度为:n(H+)=0.04moL+2×0.025moL=0.09mol,1.92g铜的物质的量为:n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,根据反应:3Cu+2NO3-+8H+=3Cu2++2NO+4H2O判断过量情况,根据不足量进行计算即可.
解答 解:100mL混合液中显示的物质的量为:n(HNO3)=0.1L×0.4mol/L=0.04mol,含有硫酸的物质的量为:n(H2SO4)=0.1L×0.25moL/L=0.025moL,溶液中氢离子浓度为:n(H+)=0.04moL+2×0.025moL=0.09mol,
1.92g铜的物质的量为:n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,
铜与硝酸发生的反应为:3Cu+2NO3-+8H+=3Cu2++2NO+4H2O
3mol 2mol 8mol
0.03mol 0.04mol 0.09mol
根据反应关系可以看出,Cu不足,氢离子和硝酸根过量,按照铜计算,
则充分反应后溶液中剩余的n(NO3-)=0.04mol-0.02mol=0.02mol,
则充分反应后溶液中c(NO3-)=$\frac{0.02mol}{0.1L}$=0.20mol/L,
故选B.
点评 本题考查物质的量浓度的计算,题目难度中等,解答该题的关键是把握反应的离子方程式,根据离子方程式判断反应物的过量情况.

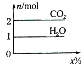 将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )| A | B | C | D | |
| 甲 | 戊烯 | 已烯 | 己二炔(C6H6) | 己烷 |
| 乙 | 环己烷(C6H12) | 苯 | 苯 | 乙醇 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氢气的燃烧热为△H=-285.5kJ•mol-1,则电解水的热化学方程式为2H2O(l)$\frac{\underline{\;电解\;}}{\;}$2H2(g)+O2(g)△H=+285.5k•Jmol-1 | |
| B. | 反应SO2(g)+2H2S(g)═3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0 | |
| C. | 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6k•Jmol-1 | |
| D. | 由C(石墨,s)=C(金刚石,s)△H=+1.90 k•Jmol-1可知,金刚石比石墨稳定 |
| A. | 在食用盐中滴加少量淀粉溶液,探究食用盐是否含有IO3- | |
| B. | 新制氯水显酸性,将其滴加到紫色石蕊溶液中,充分振荡后溶液最终为无色 | |
| C. | 氯气具有漂白性,可以将湿润的有色布条漂白为无色物质 | |
| D. | 根据较强酸可以制取较弱酸的规律,结合酸性的强弱顺序H2CO3>HClO>HCO3-,可以推出少量的CO2通入NaClO溶液中能生成HClO和碳酸钠 |
| A. | 氟化氢气体分解生成氢气和氟气的反应是放热反应 | |
| B. | 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270kJ | |
| C. | 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | |
| D. | 放热反应的反应速率总是大于吸热反应的反应速率 |
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值减小 | |
| B. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)>c(CH3COO -) | |
| C. | 常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| D. | c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c(NH4)2SO4>c(NH4Cl) |
| A. | 碘酒是指碘单质的乙醇溶液 | |
| B. | 浓硫酸可以刻蚀石英制艺术品 | |
| C. | 84消毒液的有效成分是NaClO | |
| D. | 氢氧化铝、小苏打等可用于治疗胃酸过多 |