题目内容
3.下列实验操作和数据记录都正确的是( )| A. | 用托盘天平称量时,将NaOH固体放在右盘内的纸上,称得质量为10.2g | |
| B. | 用25mL碱式滴定管量取高锰酸钾溶液,体积为16.60mL | |
| C. | 用干燥的广泛pH试纸测稀盐酸的pH=3.2 | |
| D. | 用10mL量筒量取NaCl溶液,体积为9.2mL |
分析 A.NaOH易潮解且具有强腐蚀性;
B.碱式滴定管只能量取碱性溶液;
C.广泛pH试纸的测定值是整数;
D.量筒的感量是0.1mL,量取溶液时量筒规格要等于或稍微大于量取溶液体积.
解答 解:A.NaOH易潮解且具有强腐蚀性,所以NaOH应该放置在小烧杯中称量,故A错误;
B.碱式滴定管只能量取碱性溶液,酸性高锰酸钾溶液呈酸性,要用酸式滴定管量取,故B错误;
C.广泛pH试纸的测定值是整数,所以用广泛pH试纸测稀盐酸的pH不能为3.2,故C错误;
D.量筒的感量是0.1mL,量取溶液时量筒规格要等于或稍微大于量取溶液体积,所以用10 mL量筒量取NaCl溶液,体积为9.2 mL,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器选取、物质称量等知识点,明确仪器用途、仪器感量、基本实验操作等知识点即可解答,注意含有刻度仪器的感量,题目难度不大.

练习册系列答案
相关题目
11.在胶片冲洗时可用硫代硫酸钠(Na2S2O3)做定影液,与胶片上未曝光的AgBr反应生成可溶性离子Ag(S2O3)23-.该有关过程的离子方程式不合理的是( )
| A. | H2S2O3溶液显弱酸性的原因是:H2S2O3?H++HS2O3- | |
| B. | Na2S2O3溶液显碱性的原因是:S2O32-+2 H2O?H2S2O3+2OH- | |
| C. | Na2S2O3和AgBr反应的离子方程式是:2S2O32-+AgBr?Ag(S2O3)23-+Br- | |
| D. | 定影不能在酸性较强的溶液中进行的原因是:S2O32-+2H+=S↓+SO2↑+H2O |
18.从柑橘中可提炼出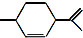 下列关于它的说法不正确的是( )
下列关于它的说法不正确的是( )
 下列关于它的说法不正确的是( )
下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | B. | 其一氯代物有8种 | ||
| C. | 能与溴水发生加成反应 | D. | 常温下呈液态,难溶于水 |
15.根据如表(部分短周期元素的原子半径及主要化合价)信息,下列叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A. | E2-与B3+的核外电子数不可能相等 | |
| B. | 离子半径大小A+<E2- | |
| C. | 最高价氧化物对应水化物的碱性A<C | |
| D. | 氢化物的稳定性H2D>H2E |
12.下列说法正确的是( )
| A. | 减小反应物浓度,可减小反应物分子中的活化分子百分数,使有效碰撞次数减小 | |
| B. | 升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 | |
| C. | 有气体参加的化学反应,若增大压强(即缩小反应容器的容积),可增加活化分子的百分数,从而使反应速率增大 | |
| D. | 催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
13.将质量为a克的铜丝在酒精灯上加热灼烧后,分别插入到下列溶液中,放置片刻,铜丝质量不变的是( )
| A. | 盐酸 | B. | 氢氧化钠 | C. | 无水乙醇 | D. | 石灰水 |
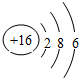 .
.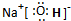 ,这种化合物形成的晶体中所含的化学键类型有离子键、共价键.
,这种化合物形成的晶体中所含的化学键类型有离子键、共价键.