题目内容
20.下列有关说法正确的是( )| A. | 根据HA、HB的电离常数的相对大小可以直接判断两种溶液的酸性强弱 | |
| B. | 常温下2S2O(g)=3S(s)+SO2(g)能自发进行,可推断该反应为放热反应 | |
| C. | 加入硫酸铜可使锌与稀硫酸的反应速率加快,说明Cu2+具有催化作用 | |
| D. | 将浓硫酸和浓硝酸混合后立即放入铁片,铁片被钝化的效果一定会更好 |
分析 A.电离受温度的影响,在同一温度下比较可以;
B.依据反应自发进行的判断依据:△H-△S<0解答;
C.加入硫酸铜可使锌与稀硫酸的反应速率加快,是因为构成原电池加快反应速率;
D.浓硫酸与浓硝酸混合,会产生大量的热.
解答 解:A.未说明溶液的温度,电离常数不能作为判断依据,故A错误;
B.由方程式2S2O(g)═3S(s)+SO2(g)可知该反应△S<0,要使△H-△S<0,必须满足△H<0,故B正确;
C.加入硫酸铜可使锌与稀硫酸的反应速率加快,是因为构成原电池加快反应速率,故C错误;
D.铁与浓硝酸或浓硫酸在冷的条件下发生钝化,浓硝酸与浓硫酸混合,放出热量,不能与铁钝化,故D错误,
故选B.
点评 本题主要考查的是酸性强弱判断、化学反应进行的方向、钝化等,难度不大,属于常考题.

练习册系列答案
相关题目
3.在所给条件下下列各组离子能够大量共存的是( )
| A. | pH=0的无色溶液中:Fe3+、Mg2+、Cl-、SO42- | |
| B. | 使甲基橙变红的溶液中:Na+、HCO3-、Cl-、NO3- | |
| C. | 在有大量MnO4-溶液中:K+、Fe2+、SO42-、Cl- | |
| D. | 投入Al有氢所放出的溶液中:Na+、Cl-、K+、SO42- |
11.2015年8月12日天津港国际物流中心内某公司的危险品仓库发生严重火灾,涉及的危险品包括压缩液化气体、电石和过氧化物等.以下灭火方法正确的是( )
| A. | 使用大量水 | B. | 使用泡沫式灭火器 | ||
| C. | 使用黄沙 | D. | 使用干粉(NaHCO3) |
8.向含有1mol KAl(SO4)2的溶液中加入适量的Ba(OH)2溶液,使SO42-恰好转化为沉淀,此时生成的Al(OH)3的物质的量是( )
| A. | 1mol | B. | 1.33mol | C. | 0.667mol | D. | 0mol |
15. (1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
(1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
浓度均为0.1mol•L-1的下列5种溶液:
①CH3COONH4 ②CH3COONa ③NaNO2 ④HF ⑤NH4Cl,
溶液pH值由小到大的顺序是(填写编号)④⑤①③②.
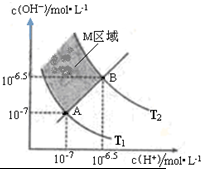
(2)如图表示某溶液中c(H+)和c(OH-)的关系,下列判断正确的是AC.
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.AB线上任意点均有pH=7
C.图中T1<T2
D.M区域内(阴暗部分)任意点均有c(H+)>c(OH-)
 (1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
(1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:| 电解质 | HF | CH3COOH | HNO2 | NH3•H2O |
| 电离平衡常数K | 3.53×10-4 | 1.76×10-5 | 4.6×10-4 | 1.77×10-5 |
①CH3COONH4 ②CH3COONa ③NaNO2 ④HF ⑤NH4Cl,
溶液pH值由小到大的顺序是(填写编号)④⑤①③②.
(2)如图表示某溶液中c(H+)和c(OH-)的关系,下列判断正确的是AC.
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.AB线上任意点均有pH=7
C.图中T1<T2
D.M区域内(阴暗部分)任意点均有c(H+)>c(OH-)
5.已知反应:KBrO3+AsH3+H2SO4--H3AsO4+K2SO4+H2O+Br2(未配平).下列叙述不正确的是( )
| A. | 反应中KBrO3得电子作氧化剂 | |
| B. | 氧化剂和还原剂的物质的量比为5:8 | |
| C. | 根据上述反应可推知,还原性:AsH3>Br2 | |
| D. | 0.2 mol KBrO3参加反应电子转移1 mol |
9.已知CaSO4受热分解,由于受热温度不同,气体成分也不同.气体成分可能为SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组准备通过系列实验探究CaSO4分解生成的气体,进而确定CaSO4分解的化学方程式.
[提出猜想]
Ⅰ.所得气体的成分可能只含 SO3一种;
Ⅱ.所得气体的成分可能含有SO2、O2 二种;(填分子式)
Ⅲ.所得气体的成分可能含有 SO2、SO3、O2三种.
[设计实验]
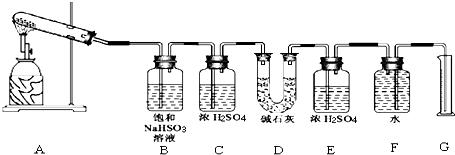
该化学课外活动小组准备通过测定D装置的增重以及量筒中水的体积,来探究CaSO4分解生成的气体成分,进而确定CaSO4分解的化学方程式.
[实验过程]
根据上述实验方案进行试验.已知实验结束时,CaSO4完全分解.
请结合以下实验现象和记录的实验数据进行分析:
(1)若实验结束时,G中量筒没有收集到水,则证明猜想Ⅰ 正确.(填Ⅰ或Ⅱ或Ⅲ)
(2)若实验结束时,装置D的总质量增加,能否断定气体产物中一定含有SO2而不含SO3?请说明理由:不能,因为SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2.
(3)该实验设计中,容易给测定带来较大误差的因素有排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差.
(写出一种即可)
(4)经改进后,有两组同学进行该实验,由于加热时的温度不同,实验测得数据也不同,
相关数据如下:
请通过计算,推断第二组同学得出的CaSO4分解的化学反应方程式:
第二组:2CaSO4$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+2SO2↑+O2↑.
[提出猜想]
Ⅰ.所得气体的成分可能只含 SO3一种;
Ⅱ.所得气体的成分可能含有SO2、O2 二种;(填分子式)
Ⅲ.所得气体的成分可能含有 SO2、SO3、O2三种.
[设计实验]
该化学课外活动小组准备通过测定D装置的增重以及量筒中水的体积,来探究CaSO4分解生成的气体成分,进而确定CaSO4分解的化学方程式.

[实验过程]
根据上述实验方案进行试验.已知实验结束时,CaSO4完全分解.
请结合以下实验现象和记录的实验数据进行分析:
(1)若实验结束时,G中量筒没有收集到水,则证明猜想Ⅰ 正确.(填Ⅰ或Ⅱ或Ⅲ)
(2)若实验结束时,装置D的总质量增加,能否断定气体产物中一定含有SO2而不含SO3?请说明理由:不能,因为SO3与B中的饱和NaHSO3反应会生成等物质的量的SO2.
(3)该实验设计中,容易给测定带来较大误差的因素有排水量气法测定气体的体积时量筒和广口瓶中液面变化和压强变化对液体体积的读数会产生误差.
(写出一种即可)
(4)经改进后,有两组同学进行该实验,由于加热时的温度不同,实验测得数据也不同,
相关数据如下:
| 实验小组 | 称取CaSO4 的质量(g) | 装置D增加 的质量(g) | 量取气体体积的装置测量的气体体积 (折算成标准状况下气体的体积) (mL) |
| 一 | 4.08 | 2.56 | 224 |
| 二 | 5.44 | 2.56 | 448 |
第二组:2CaSO4$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+2SO2↑+O2↑.
10. 实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH4++6HCHO═3H++6H2O+(CH2)6N4H+(滴定时,1mol(CH2)6N4H+与 l mol H+相当),然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ:称取样品1.500g.
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④判断滴定终点的现象是溶液由无色变为粉红,且保持半分钟不变色.
⑤如图是某次滴定时的滴定管中的液面,其读数为22.60mL.
(2)滴定结果如下表所示:
若NaOH标准溶液的浓度为0.1050mol•L-1则该样品中氮的质量分数为19.6%.
 实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4++6HCHO═3H++6H2O+(CH2)6N4H+(滴定时,1mol(CH2)6N4H+与 l mol H+相当),然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ:称取样品1.500g.
步骤Ⅱ:将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀.
步骤Ⅲ:移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化
B.锥形瓶内溶液颜色的变化
④判断滴定终点的现象是溶液由无色变为粉红,且保持半分钟不变色.
⑤如图是某次滴定时的滴定管中的液面,其读数为22.60mL.
(2)滴定结果如下表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |