2.下列实验装置进行的相应实验,能达到实验目的是( )
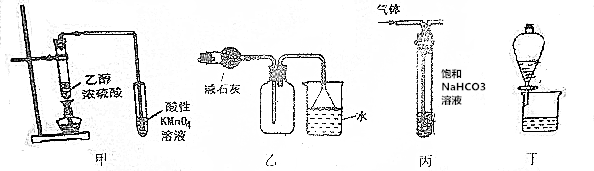

| A. | 装置甲可用于检验乙烯生成 | |
| B. | 装置乙可用于收集和吸收氨气 | |
| C. | 装置丙可用于出去CO2中混有的SO2气体 | |
| D. | 装置丁可分离碘的CCl4溶液 |
1.下列有关仪器的性能或者使用方法的说明中正确的是( )
| A. | 试管、蒸发皿既能用于给固体加热也能用于给溶液加热 | |
| B. | 分液漏斗既能用于某些混合物的分离也能用于组装气体发生装置 | |
| C. | 碱式滴定管既可用于中和滴定,也可用于量取一定量的NaCl或AlCl3溶液 | |
| D. | 测量酒精沸点的实验中,应使温度计水银球位于被加热的酒精中 |
20.高铁酸钠(Na2FeO4)是一种高效多功能水处理剂.工业上通过以下反应生产:
3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4+3NaCl+6NaNO3+5H2O
下列有关该反应的说法正确的是( )
3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4+3NaCl+6NaNO3+5H2O
下列有关该反应的说法正确的是( )
| A. | 氯元素的化合价升高 | B. | Fe(NO3)3是氧化剂 | ||
| C. | 铁元素被氧化 | D. | NaOH发生氧化反应 |
18.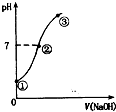 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
 常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )
常温下,向饱和氯水中逐滴滴入0.1mol•L-1的氢氧化钠溶液,pH变化如图所示,下列有关叙述正确的是( )| A. | ①点所示溶液中只存在HCl0的电离平衡 | |
| B. | ②到③的过程中水的电离程度一定减少 | |
| C. | ②点处表示氯气与氢氧化钠溶液恰好反应完全 | |
| D. | ②点所示溶液中:c( Na+)=c(HCl0)+2c(ClO -) |
17.有下列三个反应方程式:①Cl2+FeI2═FeCl2+I2 ②2Fe2++Br2═2Fe3++2Br-③Co2O3+6HCl═2CoCl2+Cl2↑+3H2O,下列说法正确的是( )
| A. | ①②③中氧化产物分别是FeCl2、Fe3+、Cl2 | |
| B. | 根据以上反应的化学方程式可以得到氧化性强弱关系为Cl2>Co2O3>Fe3+ | |
| C. | 在反应③中生成1 mol Cl2时,有2 mol HCl被氧化 | |
| D. | 根据反应①②一定可以推理得到Cl2+FeBr2═FeCl2+Br2 |
16.下列实验能够成功的是( )
| A. | 通过溴水除去甲烷中的乙炔 | |
| B. | 将乙醇加热到170℃制备乙烯 | |
| C. | 加入浓溴水后过滤除去苯中的苯酚 | |
| D. | 加入氢氧化钠后蒸馏除去乙酸乙酯中的乙酸 |
15.溶质相同、质量分数为a%和b%的两份溶液质量分别为mg、ng,将两份溶液混合并蒸发去xg水,所得溶液的物质的量浓度为c mol/L.关于求溶质的摩尔质量,下列说法正确的是( )
| A. | 只要知道蒸发后所得溶液的密度(ρ),就能求出溶质的摩尔质量 | |
| B. | 只要知道混合前两份溶液的物质的量浓度(c),就能求出溶质的摩尔质量 | |
| C. | 只要知道蒸发前混合液的体积(V),就能求出溶质的摩尔质量 | |
| D. | 以上说法都不正确 |
14.下列元素中,原子最外层电子数与其电子层数相同的有( )
| A. | H | B. | Na | C. | Al | D. | Si |
13.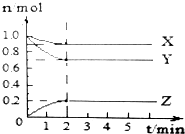 某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )
某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )
0 153858 153866 153872 153876 153882 153884 153888 153894 153896 153902 153908 153912 153914 153918 153924 153926 153932 153936 153938 153942 153944 153948 153950 153952 153953 153954 153956 153957 153958 153960 153962 153966 153968 153972 153974 153978 153984 153986 153992 153996 153998 154002 154008 154014 154016 154022 154026 154028 154034 154038 154044 154052 203614
 某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )
某温度时,在1L恒容密闭容器中X、Y、Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( )| A. | 反应开始至2min,反应的平均速率v(Z)=0.2mol/L | |
| B. | 该反应的化学方程式为X+3Y═2Z | |
| C. | 该反应平衡时,Y转化率为30% | |
| D. | 3min时,充入X,v正增大,v逆减小 |