12.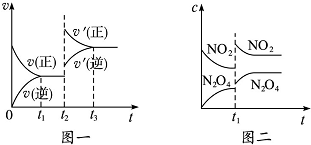 已知图一表示的是可逆反应C(s)+H2O(g)?CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)?2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )
已知图一表示的是可逆反应C(s)+H2O(g)?CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)?2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )
 已知图一表示的是可逆反应C(s)+H2O(g)?CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)?2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )
已知图一表示的是可逆反应C(s)+H2O(g)?CO(g)+H2(g)△H<0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)?2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( )| A. | 图一t2时改变的条件可能是升高了温度或增大了压强 | |
| B. | 图一t2时改变的条件是增大压强,则反应的△H增大 | |
| C. | 图二t1时改变的条件可能是升高了温度 | |
| D. | 若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将增大 |
11.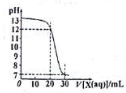 如图为用一定浓度的盐酸X滴定10mL一定浓度NaOH溶液Y的滴定图象,依据图象推出X和Y的物质的量浓度是下表内各组中的( )
如图为用一定浓度的盐酸X滴定10mL一定浓度NaOH溶液Y的滴定图象,依据图象推出X和Y的物质的量浓度是下表内各组中的( )
 如图为用一定浓度的盐酸X滴定10mL一定浓度NaOH溶液Y的滴定图象,依据图象推出X和Y的物质的量浓度是下表内各组中的( )
如图为用一定浓度的盐酸X滴定10mL一定浓度NaOH溶液Y的滴定图象,依据图象推出X和Y的物质的量浓度是下表内各组中的( )| A | B | C | D | |
| X/mol/L | 0.09 | 0.03 | 0.04 | 0.12 |
| Y/mol/L | 0.03 | 0.09 | 0.12 | 0.04 |
| A. | A | B. | B | C. | C | D. | D |
10.室温下,将0.1molK2CO3固体溶于水配成100mL溶液,向溶液中加入下列物质.有关结论正确的是( )
| 加入的物质 | 结论 | |
| A | 100mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
| B | 0.01molK2O | 溶液中$\frac{c(HC{{O}_{3}}^{-})}{c(O{H}^{-})}$ 增大 |
| C | 50mL 1mol/LH2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| D | 0.1molKHSO4固体 | 反应结束后,溶液pH=7 |
| A. | A | B. | B | C. | C | D. | D |
9.(1)根据氧化还原反应2H2+O2═2H2O,设计成燃料电池,负极通的气体应是H2,正极通的气体应是O2.
(2)根据选择电解质溶液的不同,填写下表:
(3)若把H2改为CH4,KOH作电解质,则负极反应式为CH4+10OH--8e-=CO32-+7H2O.
(2)根据选择电解质溶液的不同,填写下表:
| 电解质溶液 | H2SO4溶液 | KOH溶液 |
| 负极反应式 | ||
| 正极反应式 | ||
| 溶液的pH变化 |
7.将含有一摩尔Na2CO3的溶液逐滴入含有1.25molHCl的稀盐酸中,混合充分反应,产生气体V1,若将上述稀盐酸全部逐滴滴入Na2CO3溶液中,混合充分反应,产生气体V2.在相同条件下V1与V2之比为( )
| A. | 1:1 | B. | 2:5 | C. | 5:2 | D. | 2:3 |
6.Mg、Zn、Al三种金属的混合物与足量稀硫酸反应,生成氢气2.8L(标准状况),原三种金属的总物质的量(单位mol)可能是( )
| A. | 0.125 | B. | 0.10 | C. | 0.08 | D. | 0.20 |
5.美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是( )
0 153835 153843 153849 153853 153859 153861 153865 153871 153873 153879 153885 153889 153891 153895 153901 153903 153909 153913 153915 153919 153921 153925 153927 153929 153930 153931 153933 153934 153935 153937 153939 153943 153945 153949 153951 153955 153961 153963 153969 153973 153975 153979 153985 153991 153993 153999 154003 154005 154011 154015 154021 154029 203614
| A. | 铝钠合金的熔点比铝低 | |
| B. | 铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na) | |
| C. | 铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出 | |
| D. | m g不同组成的铝钠合金投入足量盐酸中,放出的H 2 越多,则铝的质量分数越小 |
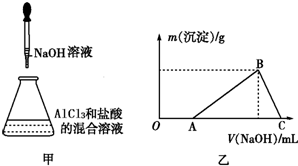 某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.
某同学称取一定质量的AlCl3固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液如图甲所示.滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示.