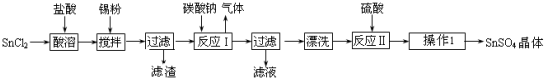
题目内容
4.化合物A是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:A(s)+H2(g)$?_{释氢}^{贮氢}$B(s)+LiH(s)△H=-44.5kJ•mol-1…①
已知:①在液氨中加入金属锂生成B和氢气;
②一定条件下,2.30g固体B与5.35gNH4Cl固体恰好完全反应,生成固体盐C和4.48L气体D(已折算成标准状况);气体D能使湿润的红色石蕊试纸变蓝色.
(1)A的化学式为Li2NH,LiH中r(Li+)小于r(H-)(填“大于”或“小于”).
(2)写出液氨与金属锂反应的化学方程式2Li+2NH3=2LiNH2+H2.
(3)B在加强热时生成NH3和另一种化合物E,该分解反应的化学方程式为3LiNH2$\frac{\underline{\;高温\;}}{\;}$Li3N+2NH3.
(4)化合物E也可以作储氢材料,其储氢原理可表示为:
E(s)+H2(g)$?_{释氢}^{贮氢}$A(s)+LiH(s)△H=-165kJ•mol-1…②
储氢材料可以通过加热的方式释放氢气.从实用化角度考虑,选择E(填“A”或“E”)作储氢材料更合理,理由是E的储氢量要比A多.
分析 在一定条件下,2.30g固体B与5.35gNH4Cl固体恰好完全反应,生成固体C和4.48L气体D(标准状况),气体D能使湿润的红色石蕊试纸变蓝色,可推知D为NH3,4.48L氨气的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,其质量=0.2mol×17g/mol=3.4g,根据质量守恒可知B的质量为2.3g+5.35g-3.4g=4.25g,NH4Cl的摩尔质量为53.5g/mol,5.35gNH4Cl为0.1mol,B中含Li,则固体B与NH4Cl固体反应可表为:B+NH4Cl→LiCl+NH3,根据Cl原子守恒,LiCl的物质的量=0.1mol,那么2.3g化合物B中含Li元素也为 0.1mol,再根据质量守恒和原子守恒(原子的种类和数目反应前后相同),则2.3gB中含有N原子为0.2mol-0.1mol=0.1mol,含有H原子为0.2mol×4-0.4mol=0.2mol,可推知B是LiNH2,液氨与金属锂反应生成氢气和LiNH2,
(1)B是LiNH2,根据A(s)+H2(g)$?_{释氢}^{贮氢}$B(s)+LiH(s),利用元素守恒可知A的化学式,离子半径大小,Li+,H-,电子层数相同,核电荷数越大半径越小;
(2)B是LiNH2,液氨与金属锂反应生成氢气和LiNH2;
(3)推知B是LiNH2,根据元素守恒可知,B在加强热时发生分解反应,生成NH3和另一种化合物E为Li3N,据此书写化学方程式;
(4)根据A和E储氢量的多少选择储氢材料.
解答 解:在一定条件下,2.30g固体B与5.35gNH4Cl固体恰好完全反应,生成固体C和4.48L气体D(标准状况),气体D能使湿润的红色石蕊试纸变蓝色,可推知D为NH3,4.48L氨气的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,其质量=0.2mol×17g/mol=3.4g,根据质量守恒可知B的质量为2.3g+5.35g-3.4g=4.25g,NH4Cl的摩尔质量为53.5g/mol,5.35gNH4Cl为0.1mol,B中含Li,则固体B与NH4Cl固体反应可表为:B+NH4Cl→LiCl+NH3,根据Cl原子守恒,LiCl的物质的量=0.1mol,那么2.3g化合物B中含Li元素也为 0.1mol,再根据质量守恒和原子守恒(原子的种类和数目反应前后相同),则2.3gB中含有N原子为0.2mol-0.1mol=0.1mol,含有H原子为0.2mol×4-0.4mol=0.2mol,可推知B是LiNH2,液氨与金属锂反应生成氢气和LiNH2,
(1)B是LiNH2,根据A(s)+H2(g)$?_{释氢}^{贮氢}$B(s)+LiH(s),利用元素守恒可知A的化学式为Li2NH,离子半径大小,Li+,H-,电子层数相同,核电荷数越大半径越小,LiH中r(Li+)小于r(H-),
故答案为:Li2NH;小于;
(2)B是LiNH2,液氨与金属锂反应生成氢气和LiNH2,反应的方程式为2Li+2NH3=2LiNH2+H2,
故答案为:2Li+2NH3=2LiNH2+H2;
(3)推知B是LiNH2,根据元素守恒可知,B在加强热时发生分解反应,生成NH3和另一种化合物E为Li3N,反应的化学方程式为3LiNH2$\frac{\underline{\;高温\;}}{\;}$Li3N+2NH3,
故答案为:3LiNH2$\frac{\underline{\;高温\;}}{\;}$Li3N+2NH3;
(4)根据A的化学式为Li2NH,E为Li3N可知,E的储氢量要比A多,所以选择选择储氢材料E比较合理,
故答案为:E,E的储氢量要比A多.
点评 本题考查无机物推断,侧重考查学生对知识的迁移应用与综合分析解决问题能力,对学生的逻辑推理有较高的要求,把握A中含Li元素,B物质化学式的推断是解题关键,难度较大.

| A. | x=4 | B. | 平衡向正反应方向移动 | ||
| C. | B的转化率降低 | D. | C的体积分数增大 |
| A. | 除去粗盐中不溶性杂质的操作有溶解、过滤、蒸发 | |
| B. | 教材上铝热反应实验中KClO3的作用是使镁带剧烈燃烧 | |
| C. | 石蜡油蒸气在炽热碎瓷片的作用下分解产生的气体可使酸性高锰酸钾溶液褪色 | |
| D. | 除去乙醇中少量的水采用加入新制的Ca(OH)2再蒸馏的方法 |
(2)根据选择电解质溶液的不同,填写下表:
| 电解质溶液 | H2SO4溶液 | KOH溶液 |
| 负极反应式 | ||
| 正极反应式 | ||
| 溶液的pH变化 |
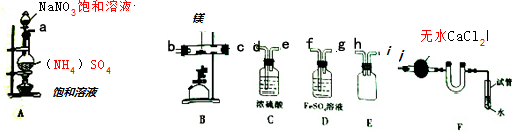
(1)装置A中反应的化学方程式为2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O.
(2)按气流方向的连接顺序是(填入仪器接口字母编号):a→( h )( i )→( f )( g )→( d )( e )→( b ) ( c )→j.
(3)装置E的作用是作安全瓶,防倒吸.
(4)能否将C与D的位置对调并说明理由否,对调后不能除去水蒸气
(5)反应过程中,装置F中的末端导管必须始终插入水中,目的是防止反应过程中空气进入硬质玻璃管
(6)请用化学方法确定是否有氮化镁生成,写出实验操作及现象取少量产物于试管中,加适量蒸馏水溶解,将湿润的红色石蕊试纸放在试管口,若试纸变蓝,证明有氮化镁生成
(7)数据记录如下:
| 空硬质玻璃管质量 | 硬质玻璃管与镁的质量 | 硬质玻璃管与产物的质量 |
| 142.312g | 142.480g | 142.550g |
②若没有装置D,请比较x与3的大小,并给出判断依据x<3,若没有装置D,氮气中混有氧气,产物中混有MgO,等质量的Mg分别与O2、N2反应时,生成MgO的质量大于Mg3N2,导致计算样品中N元素质量偏大,故因此$\frac{n(Mg)}{n(O)}$<$\frac{3}{2}$,即x<3.
| A. | NH4+可能存在 | |
| B. | 若焰色反应测得K+存在,则NH4+不一定存在 | |
| C. | Cl-不可能存在 | |
| D. | Ba2+一定不存在,Mg2+可能存在 |