13.有一支25mL酸式滴定管,其中所盛溶液液面恰好在5mL处.现将管内溶液全部排出并用量筒量得该溶液的体积为( )
| A. | 5mL | B. | 20mL | C. | >20mL | D. | <20mL |
12.家用炒菜铁锅用水清洗放置后出现红棕色的锈斑,在此变化过程中不发生的化学反应是( )
| A. | 4Fe(OH)2+2H2O+O2═4Fe(OH)3 | B. | 2Fe+2H2O+O2═2Fe(OH)2 | ||
| C. | 2H2O+O2+4e-→4OH- | D. | Fe→Fe3++3e- |
11.下列反应中,属于放热反应的是( )
| A. | 铝粉与氧化铁的反应 | B. | 氯化铵晶体与Ba(OH)2•8H2O的反应 | ||
| C. | 氯酸钾的分解反应 | D. | 盐类的水解反应 |
10.把FeCl3溶液蒸干灼烧,最后得到的固体产物是( )
| A. | FeCl3 | B. | Fe(OH)3 | C. | FeO | D. | Fe2O3 |
7.下表是不同温度下水的离子积数据:
试回答以下问题:
(1)若25<t1<t2,则α>(填“<”“>”或“=”)1×10-14,
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol•L-1,取该溶液1mL,加水稀释至10mL,则稀释后溶液中c(Na+):c(SO42-)=2:1; c(Na+):c(OH-)=1000:1.
(3)10mLpH=4的盐酸,稀释10倍到100mL时,pH=5.
(4)常温下,pH=5和pH=3的盐酸溶液等体积混合后溶液的pH=3.3.
(5)将t2℃温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
①若所得混合溶液为中性,则a:b=10:1;
②若所得混合溶液pH=2,则a:b=9:2.(以上均忽略溶液混合前后体积的变化)
| 温度(℃) | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-13 |
(1)若25<t1<t2,则α>(填“<”“>”或“=”)1×10-14,
(2)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol•L-1,取该溶液1mL,加水稀释至10mL,则稀释后溶液中c(Na+):c(SO42-)=2:1; c(Na+):c(OH-)=1000:1.
(3)10mLpH=4的盐酸,稀释10倍到100mL时,pH=5.
(4)常温下,pH=5和pH=3的盐酸溶液等体积混合后溶液的pH=3.3.
(5)将t2℃温度下pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合,
①若所得混合溶液为中性,则a:b=10:1;
②若所得混合溶液pH=2,则a:b=9:2.(以上均忽略溶液混合前后体积的变化)
6.下列有关反应进行方向的叙述中不正确的是( )
| A. | 焓变和熵变都与反应的自发性有关,又都不能独立地作为自发性的判据 | |
| B. | -10℃的液态水就会自动结冰成为固态,因为这是熵增的过程 | |
| C. | 大量事实告诉我们,过程的自发性只能用于判断过程的方向,不能确定过程是否一定会发生和过程发生的速率 | |
| D. | 放热反应过程中体系能量降低,因此有自发进行的倾向,但是有些吸热反应也可以自发进行 |
5.下列有机物中含有两种官能团的是( )
0 153787 153795 153801 153805 153811 153813 153817 153823 153825 153831 153837 153841 153843 153847 153853 153855 153861 153865 153867 153871 153873 153877 153879 153881 153882 153883 153885 153886 153887 153889 153891 153895 153897 153901 153903 153907 153913 153915 153921 153925 153927 153931 153937 153943 153945 153951 153955 153957 153963 153967 153973 153981 203614
| A. | CH2=CHCl | B. |  | C. | 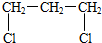 | D. | 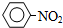 |

 (1)某同学用碳棒,铜棒,稀硫酸和干电池为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑请在右边画出能够实验这一反应的装置图.
(1)某同学用碳棒,铜棒,稀硫酸和干电池为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑请在右边画出能够实验这一反应的装置图.
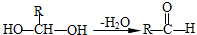

 .
.