题目内容
10.把FeCl3溶液蒸干灼烧,最后得到的固体产物是( )| A. | FeCl3 | B. | Fe(OH)3 | C. | FeO | D. | Fe2O3 |
分析 根据三氯化铁在溶液中存在水解平衡,从平衡移动的角度分析,Fe3+发生水解生成Fe(OH)3:FeCl3+3H2O?Fe(OH)3+3HCl,由于加热蒸发,使HCl挥发,得到水解产物氢氧化铁,灼烧得到氧化铁.
解答 解:在FeCl3溶液中,Fe3+发生水解生成Fe(OH)3:FeCl3+3H2O?Fe(OH)3+3HCl,由于加热蒸发,使HCl挥发,破坏平衡,使平衡不断向右移动,结果生成Fe(OH)3,又由于灼热发生2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,使Fe(OH)3分解生成Fe2O3,
故选D.
点评 本题考查盐类的水解,题目难度不大,注意水解平衡移动的影响因素.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
20.中华民族有着光辉灿烂的发明史,下列发明创造不涉及氧化还原反应的是( )
| A. | 用胆矾炼铜 | B. | 用铁矿石炼铁 | ||
| C. | 黑火药的使用 | D. | 打磨磁石制指南针 |
1. 汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.
汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.
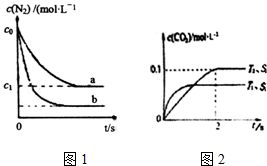
(1)汽车内燃机工作时发生反应N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T0℃时将等物质的量的N2(g)和O2(g)充入恒容密闭容器中发生反应,图1曲线a表示该反应在T0℃下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化.下列叙述正确的是ad.
a.温度T0℃下,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$
b.温度T0℃下,随着反应的进行,混合气体的密度减小
c.曲线b对应的条件改变可能是充入了NO气体
d.若曲b对应的条件改变是温度,可判断△H>0
(2)汽车安装尾气催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H.某科研小组为了探究催化剂的效果,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
①2~3s间的平均反应速率v(N2)=4.5×10-5mol•L-1•S1.
②在该温度下,反应的平衡常数K=5000.
③在使用等质量催化剂时,增大固体催化剂的表面积可提高化学反应速率.下图表示在其他条件不变时,CO2的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.由此可知该反应的△H<0(填“>”“<”),原因是温度T1到达平衡的时间短,反应速率快,故温度T2<T1,温度越高,平衡时CO2的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0.
若催化剂的表面积S1>S2,在图2中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
④假设在密闭容器中发生上述反应,达到平衡时能提高NO转化率的措施是降低反应体系的温度或缩小容器的体积.
(3)用NH3还原NOx生成N2和H2O也可以减少污染.现有NO、NO2的混合气3L,可用同温同压下3.5L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为1:3.
 汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.
汽车尾气是城市主要空气污染物,研究控制汽车尾气排放是保护环境的首要任务.(1)汽车内燃机工作时发生反应N2(g)+O2(g)?2NO(g),是导致汽车尾气中含有NO的原因之一.T0℃时将等物质的量的N2(g)和O2(g)充入恒容密闭容器中发生反应,图1曲线a表示该反应在T0℃下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化.下列叙述正确的是ad.
a.温度T0℃下,该反应的平衡常数K=$\frac{4({c}_{0}-{c}_{1})^{2}}{{{c}_{1}}^{2}}$
b.温度T0℃下,随着反应的进行,混合气体的密度减小
c.曲线b对应的条件改变可能是充入了NO气体
d.若曲b对应的条件改变是温度,可判断△H>0
(2)汽车安装尾气催化转化器可将尾气中的主要污染物转化成无毒物质,反应为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H.某科研小组为了探究催化剂的效果,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(×10-4mol•L-1) | 10.0 | 4.50 | 2.50 | 1.60 | 1.00 | 1.00 |
| c(CO)/(×10-3mol•L-1) | 3.60 | 3.05 | 2.85 | 2.76 | 2.70 | 2.70 |
②在该温度下,反应的平衡常数K=5000.
③在使用等质量催化剂时,增大固体催化剂的表面积可提高化学反应速率.下图表示在其他条件不变时,CO2的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.由此可知该反应的△H<0(填“>”“<”),原因是温度T1到达平衡的时间短,反应速率快,故温度T2<T1,温度越高,平衡时CO2的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0.
若催化剂的表面积S1>S2,在图2中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线.
④假设在密闭容器中发生上述反应,达到平衡时能提高NO转化率的措施是降低反应体系的温度或缩小容器的体积.
(3)用NH3还原NOx生成N2和H2O也可以减少污染.现有NO、NO2的混合气3L,可用同温同压下3.5L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为1:3.
18.将乙醇1mol(其中的羟基氧用 18O 标记)在浓硫酸存在并加热下与足量乙酸充分反应.下列叙述不正确的是( )
| A. | 不可能生成90g 乙酸乙酯 | B. | 生成的乙酸乙酯中含有18O | ||
| C. | 可能生成61.6g 乙酸乙酯 | D. | 生成的水分子中一定含有18O |
5.下列有机物中含有两种官能团的是( )
| A. | CH2=CHCl | B. |  | C. | 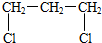 | D. | 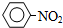 |
19. 某学生欲通过实验方法验证Fe2+的性质.
某学生欲通过实验方法验证Fe2+的性质.
(1)该同学在实验前,依据Fe2+的还原性,填写了下表.
依照表中操作,该同学进行实验.观察到液面上方气体逐渐变为红棕色,但试管中溶液颜色却变为深棕色.
为了进一步探究溶液变成深棕色的原因,该同学进行如下实验.
(2)向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者(加了数滴浓硝酸的FeSO4溶液)变红.该现象的结论是Fe2+被硝酸氧化为Fe3+.
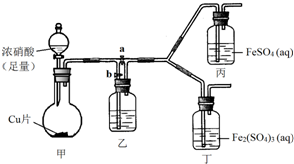
(3)该同学通过查阅资料,认为溶液的深棕色可能是NO2或NO与溶液中Fe2+或Fe3+发生反应而得到的.为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究.
ⅰ.打开活塞a、关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液无明显变化.
ⅱ.打开活塞b、关闭a,一段时间后再停止甲中反应.
ⅲ.为与ⅰ中实验进行对照,更换丙、丁后(溶质不变),使甲中反应继续,观察到的现象与步骤ⅰ中相同.
①铜与足量浓硝酸反应的化学方程式是Cu+4HNO3(浓)=Cu(NO)3+2NO2↑+2H2O;
②装置乙的作用是使NO2转化为NO;
③步骤ⅱ的目的是排出乙右侧装置中残留的NO2;
④该实验可得出的结论是溶液的深棕色是由NO或NO2与Fe2+作用得到(或不是由NO或NO2与Fe3+作用得到).
(4)该同学重新进行(1)中实验,观察到了预期现象,其实验操作是向盛有浓硝酸的试管中滴入数滴新制FeSO4溶液,振荡.
 某学生欲通过实验方法验证Fe2+的性质.
某学生欲通过实验方法验证Fe2+的性质.(1)该同学在实验前,依据Fe2+的还原性,填写了下表.
| 实验操作 | 预期现象 | 反应的离子方程式 |
| 向盛有新制FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++NO${\;}_{3}^{-}$+2H+=Fe3++NO2↑+H2O |
为了进一步探究溶液变成深棕色的原因,该同学进行如下实验.
(2)向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者(加了数滴浓硝酸的FeSO4溶液)变红.该现象的结论是Fe2+被硝酸氧化为Fe3+.
(3)该同学通过查阅资料,认为溶液的深棕色可能是NO2或NO与溶液中Fe2+或Fe3+发生反应而得到的.为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究.
ⅰ.打开活塞a、关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液无明显变化.
ⅱ.打开活塞b、关闭a,一段时间后再停止甲中反应.
ⅲ.为与ⅰ中实验进行对照,更换丙、丁后(溶质不变),使甲中反应继续,观察到的现象与步骤ⅰ中相同.
①铜与足量浓硝酸反应的化学方程式是Cu+4HNO3(浓)=Cu(NO)3+2NO2↑+2H2O;
②装置乙的作用是使NO2转化为NO;
③步骤ⅱ的目的是排出乙右侧装置中残留的NO2;
④该实验可得出的结论是溶液的深棕色是由NO或NO2与Fe2+作用得到(或不是由NO或NO2与Fe3+作用得到).
(4)该同学重新进行(1)中实验,观察到了预期现象,其实验操作是向盛有浓硝酸的试管中滴入数滴新制FeSO4溶液,振荡.
 .
.