��Ŀ����
9�����к�FeC12���ʵ��Ȼ�ͭ���壨CuCl2•2H2O����Ϊ��ȡ������CuCl2•2H2O�����Ƚ����Ƴ�ˮ��Һ��Ȼ����ͼ��ʾ��������ᴿ��
��֪H2O2��KmnO4��NaClO��K2Cr2O7������ǿ�����ԣ�Ҫ����Һ�е�Cu2+��Fe2+��Fe3+����Ϊ�����������Һ��pH�ֱ�Ϊ6.4��6.4��3.7��
��ش���������
��1����ʵ�����ʺϵ�������X��C��
A��K2Cr2O7 B��NaClO C��H2O2 D��KMnO4
��2������Y��������B��
A��CuO B��CuCl2C��Cu��OH��2D��CuCO3
��3����ȥFe3+���й����ӷ���ʽ�ǣ�����Y�ڣ�2����ѡ����ʵ�ѡ���2Fe3++3Cu��OH��2�T2Fe��OH��3+3Cu2+����
��4��������������Ŀ���ǽ�Fe2+����ΪFe3+���ٳ�ȥ��
��5������ܲ���ֱ�������ᾧ�õ�CuCl2•2H2O�����ܣ�����ܡ����ܡ������粻�ܣ�Ӧ��β����������ܣ��˿ղ��Ӧ���Ȼ���������Ũ������ȴ�ᾧ��
���� ��������ݿ�֪Fe3+������Fe��OH��3��������ȥ������������X��Ŀ���ǰ���������������Ϊ�������������ʣ�Ӧ�ù������⣻�����Լ�Y��Ŀ���ǵ���pHʹ���������������������������˳�ȥ����������Һ��������Ũ������ȴ�ᾧ�����˵õ��Ȼ�ͭ���壮
��1����������������Fe2+����ΪFe3+���׳�ȥ������ʱ�����������µ����ʣ�
��2������Y�������ǵ�����Һ��pH���ݴ���ѡ����ʵ��Լ���
��3��������ͭ�ܴٽ����������ӵ�ˮ�⣻
��4����������������Fe2+����ΪFe3+��
��5��CuCl2����ǿ�������Σ���������ʱ�ٽ���ˮ�⣨HCl�ӷ�����
��� �⣺��������ݿ�֪Fe3+������Fe��OH��3��������ȥ������������X��Ŀ���ǰ���������������Ϊ�������������ʣ�Ӧ�ù������⣻�����Լ�Y��Ŀ���ǵ���pHʹ���������������������������˳�ȥ����������Һ��������Ũ������ȴ�ᾧ�����˵õ��Ȼ�ͭ���壬
��1���������⣬����������X�ɰ�Fe2+����ΪFe3+����û�����������ʣ�����XΪH2O2��
�ʴ�Ϊ��C��
��2�������ʾ������pH��3.7��ʹFe3+ȫ������������Y���ΪCuO��Cu��OH��2��CuCO3��CuCl2���ܵ���pH��
�ʴ�Ϊ��B��
��3��Fe3+ˮ�������ԣ��й����ӷ���ʽFe3++3H2O?Fe��OH��3+3H+������������ͭ����Һ�������ӷ�Ӧ��Cu��OH��2+2H+�TCu2++2H2O��ʹˮ��ƽ��������Ӧ����һ�����ܷ�ӦʽΪ��2Fe3++3Cu��OH��2�T2Fe��OH��3+3Cu2+��
�ʴ�Ϊ��2Fe3++3Cu��OH��2�T2Fe��OH��3+3Cu2+��
��4��Fe2+����Ϊ��������ʱ����pH��Cu2+�ij�����pH��ͬ��Ҳ����˵��Fe2+������ͬʱ��Cu2+Ҳ��������������߷��뿪����������ṩ��Ϣ��֪Fe3+���������pH��С������Ӧ�Ƚ�Fe2+����ΪFe3+���ٽ����ȥ��
�ʴ�Ϊ����Fe2+����ΪFe3+���ٳ�ȥ��
��5��CuCl2����ǿ�������Σ���������ʱ�ٽ���ˮ�⣨HCl�ӷ���������Ӧ��HCl�����в���Ũ������ȴ�ᾧ�ķ������Եõ�CuCl2•2H2O�ľ��壬
�ʴ�Ϊ�����ܣ�Ӧ���Ȼ���������Ũ������ȴ�ᾧ��
���� ���⿼�����ʵķ��롢�ᴿ��ʵ����ƣ�Ϊ��Ƶ���㣬������ѧ���ķ��������Ŀ��飬��Ŀ��Ƕȿ���ѧ�����Ķ���ȡ��Ϣ�������Թ�������������ʵ���������ơ�ʵ�鷽�������ۡ����ʷ����ᴿ���ӵ��й�ʵ������Լ������龳���ۺ�����֪ʶ����������������Ŀ�Ѷ��еȣ�Ҫ��ѧ��Ҫ����ʵ��ʵ�����֪ʶ�����Ӧ����Ϣ��������������ע�����֪ʶ��ȫ�����գ�

| A�� | ������ɫ������Ӧ�����ӷ���ʽΪ��2Cu2++4I-=2CuI��+I2 | |
| B�� | ͨ��SO2����Һ�����ɫ��������SO2��Ư���� | |
| C�� | ����ʵ�������£����ʵ�������ǿ��˳��Ϊ��Cu2+��I2��SO2 | |
| D�� | �μ�KI��Һʱ��ÿ����1mol CuIת��1mol e- |
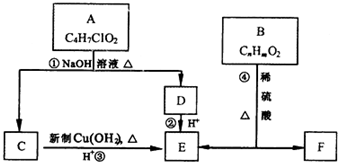
| A�� | CH3COOH | B�� | HOOC-COOH | C�� | HO��CH2��2CHO | D�� | HOC6H4COOH |
| A�� | a=b | B�� | a��b | C�� | a��b | D�� | ����ȷ�� |
| A�� | NO2 | B�� | Ba��OH��2 | C�� | Cl2 | D�� | CH3COONa |
| A�� | �Ҵ��ڵ�صĸ����ϲμӷ�Ӧ | |
| B�� | 1mol CH3CH2OH������ת��6mole- | |
| C�� | ���ŷ�Ӧ�Ľ��У��������������Լ��� | |
| D�� | ��طŵ�����л�ѧ��ת���ɵ��� |
��֪��̼��﮵��ܽ��Ϊ�� g/L��
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
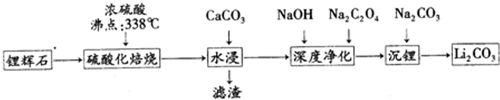
��2�����ữ���չ�ҵ��Ӧ�¶ȿ�����250-300�棬��Ҫԭ�����¶ȵ���250�棬��Ӧ���ʽ������¶ȸ���300�棬����ӷ��϶ࣻͬʱ����������Ϊ���ۺ�������115%���ң�����������������ABC������ѡ����ţ���
A����������� B�����Ӻ������ʵĴ����� C�����Ӻ����к���ĸ���
��3��ˮ��ʱ����Ҫ�ڽ����¼���ʯ��ʯ��ĩ����Ҫ�����dz�ȥ��������ᣬͬʱ����pH����ȥ�����ʣ�
��4������ﮡ��Ļ�ѧ��Ӧ����ʽΪNa2CO3+Li2SO4=Li2CO3��+Na2SO4��
��5������ﮡ���Ҫ��95�����Ͻ��У���Ҫԭ�����¶�Խ�ߣ�̼����ܽ�Ƚ��ͣ��������Ӳ��ʣ�����̼�������ĸҺ����Ҫ���������ƣ������ܺ���̼���ƺ�̼��ﮣ�
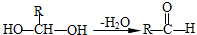

 ��
��