题目内容
13.有一支25mL酸式滴定管,其中所盛溶液液面恰好在5mL处.现将管内溶液全部排出并用量筒量得该溶液的体积为( )| A. | 5mL | B. | 20mL | C. | >20mL | D. | <20mL |
分析 滴定管的刻度从上到下逐渐增大,0刻度在上方,25mL的刻度线以下还有没有刻度的一部分,若把到5mL刻度位置的液体放出,其液体体积大于(25-5)mL,据此进行解答.
解答 解:滴定管的0刻度在上方,且25mL刻度线以下还有一段没有刻度,若把到5mL刻度位置的液体放出,则所得溶液的体积大于(25-5)mL=20mL,
故选C.
点评 本题考查了计量仪器的构造及其使用方法,题目难度不大,注意掌握常见计量仪器的构造及其正确使用方法,明确滴定管0刻度在上方,最大刻度线下方还有一段没有刻度线.

练习册系列答案
相关题目
3.下列各组离子,能在指定溶液中大量共存的是( )
| A. | 无色溶液中:Na+、MnO4-、CO32-、Cl- | |
| B. | 能使紫色石蕊试剂变红的溶液中:OH-、K+、Ba2+、Na+ | |
| C. | 透明的酸性溶液中:Fe3+、Mg2+、Cl-、NO3- | |
| D. | pH=1的溶液中:NH4+、Fe2+、Cl-、NO3- |
4.某溶液中含有HCO3-、SO32-、Na+、NO3-四种离子,向其中加入足量的Na2O2固体后,假设溶液体积无变化,溶液中离子浓度基本保持不变的是( )
| A. | NO3- | B. | HCO3- | C. | Na+ | D. | SO32- |
1.维生素C的结构简式如图,有关它的叙述错误的是( )
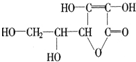

| A. | 是一个环状的酯类化合物 | B. | 易起加成及氧化反应 | ||
| C. | 可以溶解于水 | D. | 在碱性溶液中能稳定地存在 |
5.已知A、B、D、E 均为中学化学常见物质,它们之间的转化关系如图所示(部分产物略去,①②③④的反应条件相同).则A、E 可能的组合为( )
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO、C ⑥AlCl3 溶液、NH3•H2O.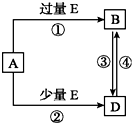
①CO2、NaOH 溶液 ②NaCl溶液、Ca(OH)2 溶液③Fe、稀HNO3 ④Na、O2 ⑤CuO、C ⑥AlCl3 溶液、NH3•H2O.

| A. | ②③④⑤ | B. | ①③④⑤⑥ | C. | ①②③⑤⑥ | D. | ①③⑤ |
3.纸是传承人类文明的载体之一.纸的主要化学成分是( )
| A. | 纤维素 | B. | 蛋白质 | C. | 塑料 | D. | 淀粉 |
 (1)某同学用碳棒,铜棒,稀硫酸和干电池为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑请在右边画出能够实验这一反应的装置图.
(1)某同学用碳棒,铜棒,稀硫酸和干电池为原材料,实现了在通常条件下不能发生的反应:Cu+H2SO4(稀)=CuSO4+H2↑请在右边画出能够实验这一反应的装置图. 某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置: