4.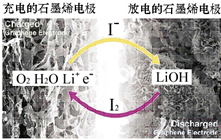 科学家开发出一种新型锂-氧电池,其能量密度极高,效率达90%以上.电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$ 2I2+4LiOH
科学家开发出一种新型锂-氧电池,其能量密度极高,效率达90%以上.电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$ 2I2+4LiOH
对于该电池的下列说法不正确的是( )
 科学家开发出一种新型锂-氧电池,其能量密度极高,效率达90%以上.电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$ 2I2+4LiOH
科学家开发出一种新型锂-氧电池,其能量密度极高,效率达90%以上.电池中添加碘化锂(LiI)和微量水,工作原理如图所示,总反应为:O2+4LiI+2H2O$?_{充电}^{放电}$ 2I2+4LiOH对于该电池的下列说法不正确的是( )
| A. | 放电时负极上I- 被氧化 | |
| B. | 充电时Li+从阳极区移向阴极区 | |
| C. | 充电时阴极反应为LiOH+e-═Li+OH- | |
| D. | 放电时正极反应为O2+2H2O+4Li++4e-═4LiOH |
3.科研、生产和生活中的下列做法,利用了氧化还原反应的是( )
| A. | 用乙醚从黄花蒿中提取青蒿素 | |
| B. | 用氯化铁溶液腐蚀铜制印刷电路板 | |
| C. | 在空气净化器中装入活性炭层 | |
| D. | 服用阿司匹林出现水杨酸反应时用小苏打解毒 |
2.下列装置所示的实验中,能达到实验目的是( )
| A. | 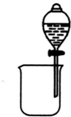 分离碘酒中的碘和酒精 | B. | 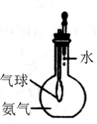 验证氨气易溶于水 | ||
| C. | 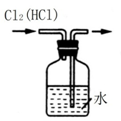 除去Cl2中的HCl杂质 | D. | 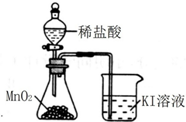 比较MnO2、Cl2、I2 |
1.下列离子方程式书写正确的是( )
| A. | Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,2Fe2++4Br-+3Cl2═2Fe2++2Br2+6Cl- | |
| B. | NaOH溶液与SO2反应,当n(NaOH):n(SO2)=4:3时,4OH-+3SO2═SO32-+2HSO3-+H2O | |
| C. | 酚酞滴入碳酸钠溶液中,溶液变红:CO32-+H2O═HCO3-+OH- | |
| D. | 将铝条投入NaOH溶液中:Al+OH-+H2O═AlO2-+H2↑ |
20.下列说法正确的是( )
| A. | 化合反应一定是氧化还原反应 | B. | 非金属氧化物一定是酸性氧化物 | ||
| C. | 金属氧化物一定是碱性氧化物 | D. | 碱性氧化物一定是金属氧化物 |
19.水的摩尔质量和1mol水的质量分别是( )
| A. | 18,18 | B. | 18g,18g | C. | 18g/mol,18g | D. | 18g,18g/mol |
18.对下列物质的分类正确的是( )
| A. | 稀盐酸属于纯净物 | B. | SO2属于酸性氧化物 | ||
| C. | 纯碱属于碱 | D. | Mn2O7属于碱性氧化物 |
17.阿伏加德罗常数的准确值是( )
| A. | 12g12C所含有的碳原子数 | B. | 1mol水中电子数 | ||
| C. | 6.02×1023 | D. | 6.02×10-23 |
15.下列有关化工生产的叙述正确的是( )
0 153435 153443 153449 153453 153459 153461 153465 153471 153473 153479 153485 153489 153491 153495 153501 153503 153509 153513 153515 153519 153521 153525 153527 153529 153530 153531 153533 153534 153535 153537 153539 153543 153545 153549 153551 153555 153561 153563 153569 153573 153575 153579 153585 153591 153593 153599 153603 153605 153611 153615 153621 153629 203614
| A. | 合成氨生产过程中将NH3液化分离,减小氨气的浓度会导致化学平衡向左移动 | |
| B. | 合成氨工业中,使用铁催化剂可加快正反应速率,提高N2、H2的转化率 | |
| C. | 电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 | |
| D. | 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小 |
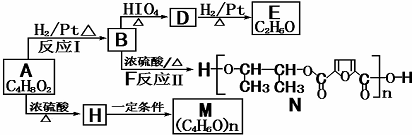
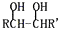 $→_{△}^{HIO_{4}}$RCHO+OHCR′
$→_{△}^{HIO_{4}}$RCHO+OHCR′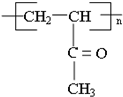
 .
.