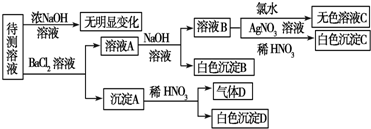
1.某混合溶液中可能含有下列离子中的若干种:Na+、K+、Fe2+、Fe3+、SO42-、CO32- 现取三份该溶液进行如下实验:
(1)第一份加入足量盐酸,无任何气体产生;
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧、最后得到红棕色固体;
(3)第三份滴加0.1mol.L-1酸性KMnO4溶液,KMnO4溶液的紫色消失
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
根据上述实验,以下说法正确的是( )
(1)第一份加入足量盐酸,无任何气体产生;
(2)第二份加入足量NaOH溶液,经搅拌、过滤、洗涤、灼烧、最后得到红棕色固体;
(3)第三份滴加0.1mol.L-1酸性KMnO4溶液,KMnO4溶液的紫色消失
(4)另用洁净的铂丝蘸取该混合溶液置于浅色火焰上灼烧,发现火焰呈现黄色.
根据上述实验,以下说法正确的是( )
| A. | 原混合溶液中只存在Na+、Fe3+、SO42-,不可能存在K+、CO32- | |
| B. | 由实验(1)无法推断原混合溶液中是否含有SO42- | |
| C. | 由实验(2)无法推断原混合溶液中是否含有Fe3+ | |
| D. | 由实验(3)可推断原混合溶液中存在Fe2+ |
19.下列物质中不含非极性共价键的是( )
①Na2O2 ②CCl4 ③HCN ④CH2=CH2 ⑤CH3COOH ⑥NaOH.
①Na2O2 ②CCl4 ③HCN ④CH2=CH2 ⑤CH3COOH ⑥NaOH.
| A. | ①②③④ | B. | ④⑤⑥ | C. | ②③⑤⑥ | D. | ①③⑤ |
17.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 室温下,12gC60和C70的混合物中含有的碳原子数为NA | |
| B. | 22.4L SO2气体中含有的氧原子数为2NA | |
| C. | 1.0L 1.0mol•L-1CH3COOH溶液中含有的CH3COOH分子数为NA | |
| D. | 标准状况下,5.6LCCl4含有的分子数为0.25NA |
16.下列元素-定为主族元素的是( )
| A. | 其原子最外电子层有7个电子的元素 | |
| B. | 最高正价为+3的元素 | |
| C. | 其原子最外层电子数大于电子层的元素 | |
| D. | 最高价氧化物对应的水化物是酸的元素 |
15.环己双妥明是一种新型的纤维酸类降脂新药,可由有机物X通过一步反应而制得:
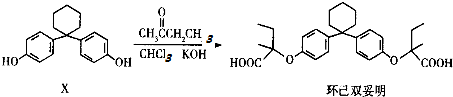
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A. | 有机物X的分子式为C18H22O2 | |
| B. | 有机物X与环己双妥明互为同系物 | |
| C. | 环己双妥明苯环上的一氯代物有4种 | |
| D. | 环己双妥明能与碳酸氢钠溶液发生反应 |
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol Cl2溶于水中,转移的电子数目为0.1NA | |
| B. | 标准状况下,2.24L CH3Cl含有的质子数目是2.3NA | |
| C. | 25℃时,1L pH=4的CH3COOH溶液中,水电离出的H+数目为10-4NA | |
| D. | 标准状况下,4.48L NO与2.24L O2混合后,所得气体中含有原子数目为0.6NA. |
12.已知S(s)=S(g)△H1,S(g)+O2(g)═SO2(g)△H2,则S(s)燃烧的热化学方程式为( )
0 153323 153331 153337 153341 153347 153349 153353 153359 153361 153367 153373 153377 153379 153383 153389 153391 153397 153401 153403 153407 153409 153413 153415 153417 153418 153419 153421 153422 153423 153425 153427 153431 153433 153437 153439 153443 153449 153451 153457 153461 153463 153467 153473 153479 153481 153487 153491 153493 153499 153503 153509 153517 203614
| A. | S(s)+O2(g)═SO2(g)△H=△H2-△H1 | |
| B. | S(s)+O2(g)═SO2(g)△H=△H1-△H2 | |
| C. | S(s)+O2(g)═SO2(g)△H=△H2+△H1 | |
| D. | 1molS(s)燃烧生成1molSO2(g)放出的热量大于1molS(g)燃烧生成1molSO2(g)放出的热量 |