题目内容
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 0.1mol Cl2溶于水中,转移的电子数目为0.1NA | |
| B. | 标准状况下,2.24L CH3Cl含有的质子数目是2.3NA | |
| C. | 25℃时,1L pH=4的CH3COOH溶液中,水电离出的H+数目为10-4NA | |
| D. | 标准状况下,4.48L NO与2.24L O2混合后,所得气体中含有原子数目为0.6NA. |
分析 A、氯气和水的反应为可逆反应;
B、求出一氯甲烷的物质的量,然后根据一氯甲烷中含26个质子;
C、在酸溶液中,氢离子绝大多数来自于酸的电离;
D、求出混合气体的物质的量,然后根据NO和氧气均为双原子分子.
解答 解:A、氯气和水的反应为可逆反应,故0.1mol氯气转移的电子数小于0.1NA个,故A错误;
B、标况下2.24L一氯甲烷的物质的量为0.1mol,而一氯甲烷中含26个质子,故0.1mol一氯甲烷中含2.6mol质子即2.6NA个,故B错误;
C、在酸溶液中,氢离子绝大多数来自于酸的电离,水的电离被抑制,故此溶液中水电离出的氢离子小于10-4NA个,故C错误;
D、标况下4.48LNO和2.24L氧气的物质的量分别为0.2mol和0.1mol,而NO和氧气均为双原子分子,故混合后所得的气体中含有的原子的物质的量仍为0.6mol即0.6NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
4.有关合金的叙述正确的是( )
| A. | 合金的导电性比成分金属强 | |
| B. | 合金的抗腐蚀性能都很好 | |
| C. | 合金的机械强度比各成分金属小 | |
| D. | 多数合金比成分金属熔点低,硬度大 |
5.2015年9月18日,美国环保署EPA宣布,大众汽车公司利用软件隐瞒了汽车有毒污染物的真实排放量,汽车尾气中的污染物有固体悬浮微粒、一氧化碳、碳氢化合物、氮氧化合物、铅及硫氧化合物等.下列有关说法中正确的是( )
| A. | 一氧化碳、氮氧化物是酸雨形成的主要因素 | |
| B. | 汽车尾气可通过净化装置将碳氢化合物还原成CO2和H2O | |
| C. | 含铅化合物导致人体蛋白质变性是物理变化 | |
| D. | 固体悬浮微粒是造成雾霾天气的一种重要因素 |
2.化合物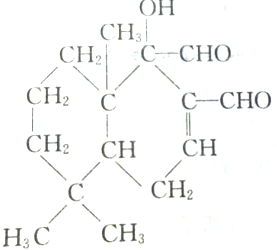 所含官能团有( )
所含官能团有( )
 所含官能团有( )
所含官能团有( )| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
9.短周期元素A、B、C、D的原子序数依次递增,它们的核电荷数之和为32,原子最外层电子数之和为10,A与C同主族,B与D同主族,A、C原子的最外层电子数之和等于B原子的次外层电子数,下列有关叙述正确的是( )
| A. | D元素处于元素周期表中第二周期VIA族 | |
| B. | 四种元素的原子半径:A<B<C<D | |
| C. | B、D的最高价氧化物具有相似的物理性质和化学性质 | |
| D. | 一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
19.下列物质中不含非极性共价键的是( )
①Na2O2 ②CCl4 ③HCN ④CH2=CH2 ⑤CH3COOH ⑥NaOH.
①Na2O2 ②CCl4 ③HCN ④CH2=CH2 ⑤CH3COOH ⑥NaOH.
| A. | ①②③④ | B. | ④⑤⑥ | C. | ②③⑤⑥ | D. | ①③⑤ |
7.下列说法正确的是( )
| A. | 加入过量氨水,有白色沉淀生成,则原溶液一定有Al3+ | |
| B. | 向某溶液中滴加稀盐酸,生成的无色无味气体能使澄清的石灰水变浑浊,则原溶液中一定含有CO32- | |
| C. | 加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO42- | |
| D. | 向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 |
5.下列过程与加成反应无关的是( )
| A. | 苯与溴水混合振荡,水层颜色变浅 | |
| B. | 乙炔与氢气反应变成乙烷 | |
| C. | 乙烯与水在一定条件下反应制取乙醇 | |
| D. | 乙烯与HCl在一定条件下反应制取氯乙烷 |