18.科学家在《Science》上发表论文,宣布发现了铝的超原子结构Al13和Al14,Al13、Al14的性质很像现行周期表中的某主族元素,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定到Al13-和Al142+.下列说法错误的是( )
| A. | Al14和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑ | |
| B. | Al13超原子中Al原子间是通过共价键结合的 | |
| C. | Al14、Al13性质与Al相似,都具有较强的还原性 | |
| D. | Al13和Al14互为同位素 |
15.元素周期表是学习化学的重要工具,它包含了许多的信息和规律.下表是元素周期表的一部分,请从下表①~⑧十种元素中选择适当的元素回答下列问题:
(1)原子半径最大的元素在周期表中的位置是第三周期第IA族.
(2)③⑦⑧三元素与①形成的气态氢化物稳定性最差的是H2S(填化学式).
(3)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是Al(OH)3,(填写化学式),该氢氧化物呈两性的原因:H++AlO2-+H2O?Al(OH)3?Al3++3OH-.(用电离方程式表示)
(4)元素⑥和Fe比较,金属性较强的元素是Al(填元素符号)用一个化学反应可以证明元素⑥和Fe的金属性的强弱,写出该反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 族 周期 | I A | II A | III A | IV A | VA | VI A | VII A |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)③⑦⑧三元素与①形成的气态氢化物稳定性最差的是H2S(填化学式).
(3)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是Al(OH)3,(填写化学式),该氢氧化物呈两性的原因:H++AlO2-+H2O?Al(OH)3?Al3++3OH-.(用电离方程式表示)
(4)元素⑥和Fe比较,金属性较强的元素是Al(填元素符号)用一个化学反应可以证明元素⑥和Fe的金属性的强弱,写出该反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
14.下列物质不能通过化合反应得到的是( )
| A. | Fe (OH)3 | B. | FeCl2 | C. | FeS | D. | Al(OH)3 |
13.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法中正确的是( )
| A. | 可能有甲烷 | B. | 一定有乙烯 | C. | 可能有丙炔 | D. | 一定无C4H4 |
12.设阿伏加德罗常数为NA.则下列说法正确的是( )
| A. | 常温常压下,11.2L甲烷中含有的氢原子数为2NA | |
| B. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| C. | 高温下,16.8g铁与足量的水蒸气充分反应,失去的电子数为0.8NA | |
| D. | 标准状况下,2.24L戊烷所含分子数为0.1NA |
11.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | C4H8 | C. | C2H4 | D. | C2H4Cl2 |
10.如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )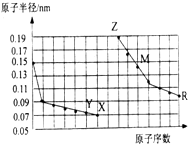
0 153079 153087 153093 153097 153103 153105 153109 153115 153117 153123 153129 153133 153135 153139 153145 153147 153153 153157 153159 153163 153165 153169 153171 153173 153174 153175 153177 153178 153179 153181 153183 153187 153189 153193 153195 153199 153205 153207 153213 153217 153219 153223 153229 153235 153237 153243 153247 153249 153255 153259 153265 153273 203614

| A. | 简单离子的半径大小比较:Z>Y>X | |
| B. | 气态氢化物稳定性:Y>X>R | |
| C. | 单质的熔点:M>Z | |
| D. | Z单质能从M的盐溶液中置换出单质M |
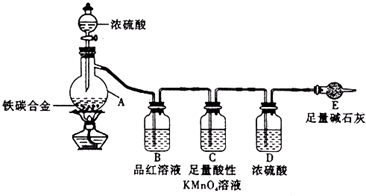
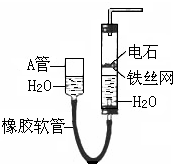 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空: .
.