题目内容
18.科学家在《Science》上发表论文,宣布发现了铝的超原子结构Al13和Al14,Al13、Al14的性质很像现行周期表中的某主族元素,当这类超原子具有40个价电子(对于主族元素的原子,外围电子又称为价电子)时最稳定,在质谱仪上可检测到稳定到Al13-和Al142+.下列说法错误的是( )| A. | Al14和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑ | |
| B. | Al13超原子中Al原子间是通过共价键结合的 | |
| C. | Al14、Al13性质与Al相似,都具有较强的还原性 | |
| D. | Al13和Al14互为同位素 |
分析 A.质谱仪检测到稳定的Al13-和Al142+等,Al14有42个价电子,极易失去2个电子成稳定的Al142+,与第二主族性质相似;
B.质谱仪检测到稳定的Al13-和Al142+等,Al13有39个价电子,极易得一个电子成稳定的Al13-,与第七主族性质相似,为分子晶体;
C.由B分析可知,Al13具有较强的氧化性;
D.同位素研究对象为原子.
解答 解:A.质谱仪检测到稳定的Al13-和Al142+等,Al14有42个价电子,极易失去2个电子成稳定的Al142+,与第二主族性质相似,Al14具有较强的还原性,和稀盐酸反应的化学方程式可表示为Al14+2HCl→Al14Cl2+H2↑,故A正确;
B.质谱仪检测到稳定的Al13-和Al142+等,Al13有39个价电子,极易得一个电子成稳定的Al13-,与第七主族性质相似,为分子晶体,Al13超原子中Al原子间是通过共价键结合的,故B正确;
C.由A中分析可知Al14具有较强的还原性,由B分析可知,Al13具有较强的氧化性,故C错误;
D.同位素研究对象为原子,Al13和Al14均不是原子,二者不是同位素关系,故D错误,
故选:CD.
点评 本题是一定信息题,是对学生信息的提取、阅读能力及综合能力考查,难度中等,是一道不错的能力考查题,关键是对信息的理解.

练习册系列答案
相关题目
3.下列鉴别方法不可行的是( )
| A. | 用水鉴别乙醇、甲苯和溴苯 | |
| B. | 用溴水鉴别植物油和己烷 | |
| C. | 用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 | |
| D. | 用酸性高锰酸钾溶液鉴别苯、环己烯和己烷 |
9.把含有某一氯化物杂质的氯化钙5.55克溶于水后,与足量的硝酸银溶液反应,生成的氯化银沉淀15克,则该杂质可能是( )
| A. | 氯化钠 | B. | 氯化钾 | C. | 氯化铜 | D. | 氯化铝 |
13.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法中正确的是( )
| A. | 可能有甲烷 | B. | 一定有乙烯 | C. | 可能有丙炔 | D. | 一定无C4H4 |
3.按混合物、电解质和非电解质顺序排列的一组物质是( )
| A. | 漂白粉、氯化钾、硫酸钡 | B. | 氯水、次氯酸钠、乙醇 | ||
| C. | 液氯、胆矾、干冰 | D. | 重水、烧碱、水 |
7.下列叙述中不正确的是( )
| A. | 一定浓度的醋酸钠溶液可使酚酞溶液变红,其原因是发生了如下反应:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) | |
| B. | 在常温下,10 mL 0.2 mol•L-1盐酸与10 mL 0.2 mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=13 | |
| C. | 在0.1 mol•L-1 NH4Cl溶液中:c(H+)+c(NH4+=c(Cl-) | |
| D. | 5 mL 1 mol•L-1 CH3COONa溶液与5 mL 1 mol•L-1盐酸混合液中c(Cl-)=c(Na+)>c(H+)>c(OH-) |
8.实验是化学研究的基础,下列是在实验室中完成的不同的化学实验,其中能达到实验目的是( )
| A. | 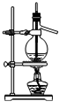 石油的分馏 | B. | 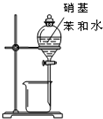 分离硝基苯和水 | ||
| C. | 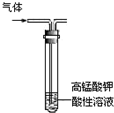 除去甲烷中的乙烯 | D. | 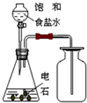 制取并收集乙炔气体 |