题目内容
11.下列分子式表示的物质一定是纯净物的是( )| A. | C5H10 | B. | C4H8 | C. | C2H4 | D. | C2H4Cl2 |
分析 纯净物是由同一种物质组成,若分子式不存在同分异构体,则该分子表示的为纯净物,根据分子式是否存在同分异构体进行解答;同分异构体是指分子式相同,但结构不同的化合物.
解答 解:A.C5H10可以表示烯烃,也可以表示环烷烃,存在多种同分异构体,不能表示纯净物,故A错误;
B.C4H8可以表示烯烃,也可以表示环烷烃,存在多种同分异构体,不能表示纯净物,故B错误;
C.C2H4只能表示乙烯,属于纯净物,故C正确;
D.C2H4Cl2中2个氯原子可以连接在同一碳原子上,为1,1-二氯乙烷,每个碳原子分别连接1个氯原子,为1,2-二氯乙烷,不能表示纯净物,故D错误;
故选C.
点评 本题以纯净物为载体考查了同分异构现象,题目难度不大,注意纯净物必须是由同一种物质组成,明确同分异构体的书写方法为解答关键,试题培养了学生的灵活应用能力.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
16.将氯化钠、氯化亚铁、氯化铁、氯化镁四种溶液,通过一步实验就能加以区别,并只用一种试剂,这种试剂是( )
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | HCl |
19.两种气态烃以任意比例混合,在105℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L.下列各组混合烃中不符合此条件的是( )
| A. | CH4 C2H4 | B. | CH4 C3H4 | C. | C2H4 C3H4 | D. | C2H2 C3H6 |
3.按混合物、电解质和非电解质顺序排列的一组物质是( )
| A. | 漂白粉、氯化钾、硫酸钡 | B. | 氯水、次氯酸钠、乙醇 | ||
| C. | 液氯、胆矾、干冰 | D. | 重水、烧碱、水 |
1.硫代硫酸钠是重要的还原剂,可用作含氮尾气处理剂、媒染剂、漂白剂等,利用重晶石生产中的副产品液态硫化钠(Na2S,含少量Na2SO3、Na2CO3及不溶性杂质)生产硫代硫酸钠的工艺流程如下:
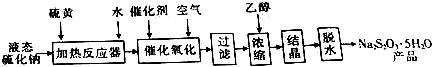
回答下列问题:
(1)反应器中Na2S与S按物质的量之比1:1反应的离子方程式为S2-+S=2S2-,反应器需加热的目的是使Na2S与S能充分反应
(2)氧化时,加入催化剂[m(MnSO4):m(NiSO4•7H2O)=1:4],测得不同温度下完全氧化所需时间如表:
氧化时适宜的操作温度为20℃~30℃,在50℃时,氧化完全所需时间比40℃时长得多,其原因是NiSO4•7H2O失去结晶水,而使催化剂的催化作用减弱
(3)过滤时,滤渣的主要成分为硫及液态硫化钠原料中的杂质,浓缩时加入适量乙醇的目的是减小Na2S2O3的溶解度.

回答下列问题:
(1)反应器中Na2S与S按物质的量之比1:1反应的离子方程式为S2-+S=2S2-,反应器需加热的目的是使Na2S与S能充分反应
(2)氧化时,加入催化剂[m(MnSO4):m(NiSO4•7H2O)=1:4],测得不同温度下完全氧化所需时间如表:
| 溶液温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 氧化完全所需时间/h | 6 | 5.5 | 5.5 | 6 | 20 | 16 | 11 | 11 |
(3)过滤时,滤渣的主要成分为硫及液态硫化钠原料中的杂质,浓缩时加入适量乙醇的目的是减小Na2S2O3的溶解度.
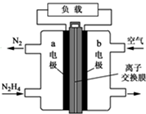 肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如上图所示,回答下列问题:
肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如上图所示,回答下列问题: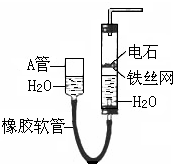 如图中的实验装置可用于制取乙炔.请填空:
如图中的实验装置可用于制取乙炔.请填空: .
.