题目内容
17.某烃的蒸气密度为3.214g/L(标准状况).该烃3.6g充分燃烧,可得5.4g水和5.6L二氧化碳(标准状况).(1)求该有机物的分子式.
(2)写出该有机物可能的结构简式.
分析 根据M=ρVm计算烃的摩尔质量,再根据计算烃、二氧化碳、水的物质的量,根据原子守恒确定该有机物分子式,书写可能的结构简式.
解答 解:(1)标准状况下,烃的蒸气密度为3.214g/L,则烃的摩尔质量为3.214g/L×22.4L/mol=72g/mol,该烃3.6g烃的物质的量为$\frac{3.6g}{72g/mol}$=0.05mol,燃烧生成水为$\frac{5.4g}{18g/mol}$=0.3mol,生成二氧化碳为$\frac{5.6L}{22.4L/mol}$=0.25mol,则烃分子中N(C)=$\frac{0.25mol}{0.05mol}$=5、N(H)=$\frac{0.3mol×2}{0.05mol}$=12,故该烃的分子式为C5H12,
答:该烃的分子式为C5H12;
(2)该有机物可能的结构简式:CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、(CH3)4C,
答:该有机物可能的结构简式:CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、(CH3)4C.
点评 本题考查有机物分子式确定、同分异构体书写,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
2.下列说法正确的( )
| A. | 纤维素、聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 用卤水点豆腐与黄河入海口处沙洲的形成,都体现了胶体聚沉的性质 | |
| C. | 用活性炭为有色物质脱色和用漂白粉漂白有色物质,原理相似 | |
| D. | 为增强84消毒液的消毒效果,使用时可加入浓盐酸 |
8.探究新制饱和氯水成分的实验时,由实验现象得出的结论错误的是( )
| A. | 向氯水中滴加NaHCO3,有气泡产生,说明氯水中含有HCl和HClO | |
| B. | 向FeCl2溶液中滴加氯水,溶液变成棕黄色,说明氯水中含有HClO | |
| C. | 氯水呈浅黄绿色,说明氯水中含有Cl2 | |
| D. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含Cl- |
12.设阿伏加德罗常数为NA.则下列说法正确的是( )
| A. | 常温常压下,11.2L甲烷中含有的氢原子数为2NA | |
| B. | 分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| C. | 高温下,16.8g铁与足量的水蒸气充分反应,失去的电子数为0.8NA | |
| D. | 标准状况下,2.24L戊烷所含分子数为0.1NA |
6.下列述叙正确的是( )
| A. | 要除去氯化镁酸性溶液里少量的氯化铁,可以选用氢氧化钠 | |
| B. | 镀锡铁表面有划痕是,仍然能阻止铁被氧化 | |
| C. | 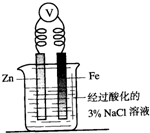 向图烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,一段时间后可看到Fe电极附近有蓝色沉淀生成 | |
| D. | 各种原生铜的硫化物经氧化、淋滤作用变成硫酸铜,遇到深层的ZnS和PbS,便慢慢地使之转变为CuS |
7.下列物质肯定为纯净物的是( )
| A. | 汽油 | B. | C2H4 | C. | 聚乙烯 | D. | 福尔马林 |