19.将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)?NH3(g)+HI(g) ②2HI(g)?H2(g)+I2(g).达到平衡时,c(H2)=1mol•L-1,c(HI)=4mol•L-1,则此温度下反应①的平衡常数为( )
| A. | 22 | B. | 24 | C. | 20 | D. | 25 |
18.在酸性溶液中能大量共存而且为无色透明的溶液是( )
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、NO3-、CO32- | ||
| C. | K+、MnO4-、NH4+、NO3- | D. | H+,K+,OH-,NO3- |
16. t℃时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
t℃时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
(1)计算t℃时该反应平衡常数的值为K=1
(2)计算该反应在0-3min时间内产物Z的平均反应速率:0.117mol/L•min,
(3)容器内混合气体的平均相对分子质量比起始投料时增大,(填“增大”、“减小”或“不变”)
(4)16min后,改变的条件为加入Y3.24mol,(注明物质的量)
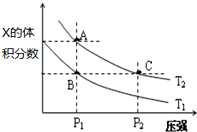
(5)在温度为T1、T2时,平衡体系中Z的体积分数随压强的变化如图所示,
①下列措施一定能增大该反应正反应速率的是ad,一定能使平衡向正反应方向移动的是cd.
a.升高温度 b.保持容器体积不变,充入惰性气体
c.分离出Z物质 d.缩小容器体积增大压强
②A和C点的正反应速率大小关系为vA<vC T2温度时,B点的正反应速率和逆反应速率大小关系为v正=v逆.
 t℃时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.
t℃时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示.| t/min | X/mol | Y/mol | Z/mol |
| 0 | 2.00 | 4.00 | 0 |
| 1 | 1.80 | 3.60 | 0.40 |
| 3 | 1.65 | 3.30 | 0.70 |
| 5 | 1.55 | 3.10 | 0.90 |
| 14 | 1.00 | 2.00 | 2.00 |
| 16 | 1.00 | 2.00 | 2.00 |
| 20 | 0.50 | 4.24 | 3.00 |
| 22 | 0.50 | 4.24 | 3.00 |
(2)计算该反应在0-3min时间内产物Z的平均反应速率:0.117mol/L•min,
(3)容器内混合气体的平均相对分子质量比起始投料时增大,(填“增大”、“减小”或“不变”)
(4)16min后,改变的条件为加入Y3.24mol,(注明物质的量)
(5)在温度为T1、T2时,平衡体系中Z的体积分数随压强的变化如图所示,
①下列措施一定能增大该反应正反应速率的是ad,一定能使平衡向正反应方向移动的是cd.
a.升高温度 b.保持容器体积不变,充入惰性气体
c.分离出Z物质 d.缩小容器体积增大压强
②A和C点的正反应速率大小关系为vA<vC T2温度时,B点的正反应速率和逆反应速率大小关系为v正=v逆.
15.已知恒容条件下,反应A2(g)+2B2(g)?2AB2(g)△H<0,下列说法正确的是( )
| A. | 升高温度,正向反应速率增加,逆向反应速率减小 | |
| B. | 达到平衡后,充入氦气,反应速率增大 | |
| C. | 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动 | |
| D. | 达到平衡后,增大A2(g)的浓度,B2的转化率增大 |
14.在2A(g)+B(g)?3C(g)+5D(g)反应中,表示该反应速率最快的是( )
0 152659 152667 152673 152677 152683 152685 152689 152695 152697 152703 152709 152713 152715 152719 152725 152727 152733 152737 152739 152743 152745 152749 152751 152753 152754 152755 152757 152758 152759 152761 152763 152767 152769 152773 152775 152779 152785 152787 152793 152797 152799 152803 152809 152815 152817 152823 152827 152829 152835 152839 152845 152853 203614
| A. | v(A)=0.5 mol/(L•s) | B. | v(B)=0.3 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(D)=0.4 mol/(L•s) |
 铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO). 杂化轨道类型sp2
杂化轨道类型sp2 杂化轨道类型sp3.
杂化轨道类型sp3.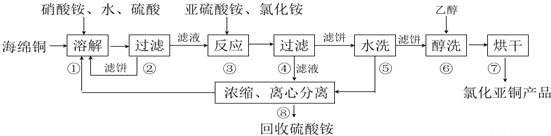
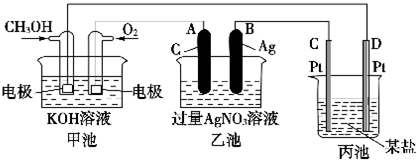
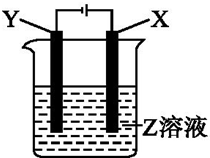 根据如图所示装置回答:
根据如图所示装置回答: