10.设阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 1mol Na2O2中阴、阳离子的总数是4NA | |
| B. | 常温常压下,11.2 LCO2所含的原子数为1.5NA | |
| C. | 标准状况下,54g H2O中含有分子数为3NA | |
| D. | 1mol/L的MgCl2溶液中Cl-离子数为2NA |
9.已知A2On2-可将B2-氧化为B单质,A2On2-则被还原为A3+,又知100mL的0.3mol/L的A2On2-与150mL的0.6mol/L B2-恰好完全反应,则A2On2-中的n值为( )
| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
8.下列反应中属于同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应的是( )
| A. | 3Br2+6KOH═5KBr+KBrO3+3H2O | |
| B. | MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+2H2O+Cl2↑ | |
| C. | 2KNO3 $\frac{\underline{\;\;△\;\;}}{\;}$ 2KNO2+O2↑ | |
| D. | NH4NO3 $\frac{\underline{\;\;△\;\;}}{\;}$ N2O↑+2H2O |
7.在实验室中,对下列事故或药品的处理正确的是( )
| A. | 金属钠着火燃烧时,用泡沫灭火器灭火 | |
| B. | 凡是给玻璃仪器加热,都要加垫石棉网,以防止仪器炸裂 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 取用化学药品时,应特别注意观察药品包装容器上的安全警示标志 |
5.工业上回收利用某合金废料(主要含Fe、Cu、Al、Co、Li等,已知Co、Fe都是中等活泼金属)的工艺流程如下:
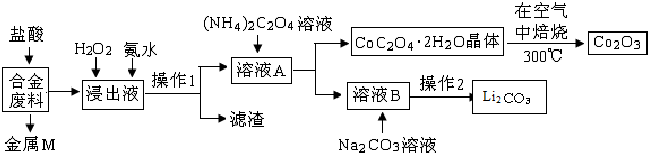
已知:Ksp[Cu(OH)2]=4.0×10-21,Ksp[Al(OH)3]=1.0×10-32,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Fe(OH)2]=8.0×10-19.pH=7.3时Li+或Co3+开始沉淀.
(1)金属M为Cu.
(2)①加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O.
②氨水的作用是调节溶液的pH,室温下,使溶液中杂质离子刚好沉淀完全而全部除去(浓度小于1.0×10-5mol•L-1).需调节溶液pH范围为5.0<pH<7.3.
(3)充分焙烧的化学方程式为4CoC2O4?2H2O+3O2$\frac{\underline{\;焙烧\;}}{\;}$2Co2O3+8 H2O+8CO2.
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失.
(5)用惰性电极电解熔融Li2CO3制取锂,阳极生成两种气体,则阳极的电极反应式为2CO32--4e-=O2↑+CO2↑.
(6)①用Li、Co形成某锂离子电池的正极是LiCoO2,含Li+导电固体为电解质.充电时,Li+还原为Li,并以原子形式嵌入电池负极材料碳-6(C6)中(如图a).电池反应为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2,
写出该电池放电时的负极反应式LixC6-xe-=C6+xLi+.
②锂硫电池的总反应为:2Li+S$?_{充电}^{放电}$Li2S,图b表示用锂离子电池给锂硫电池充电,请在图b的电极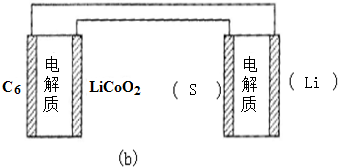 中填写“Li”或“S”,以达到给锂硫电池充电的目的.
中填写“Li”或“S”,以达到给锂硫电池充电的目的.
0 152306 152314 152320 152324 152330 152332 152336 152342 152344 152350 152356 152360 152362 152366 152372 152374 152380 152384 152386 152390 152392 152396 152398 152400 152401 152402 152404 152405 152406 152408 152410 152414 152416 152420 152422 152426 152432 152434 152440 152444 152446 152450 152456 152462 152464 152470 152474 152476 152482 152486 152492 152500 203614

已知:Ksp[Cu(OH)2]=4.0×10-21,Ksp[Al(OH)3]=1.0×10-32,Ksp[Fe(OH)3]=1.0×10-38,Ksp[Fe(OH)2]=8.0×10-19.pH=7.3时Li+或Co3+开始沉淀.
(1)金属M为Cu.
(2)①加入H2O2的作用是(用离子方程式表示)2Fe2++H2O2+2H+=2Fe3++2H2O.
②氨水的作用是调节溶液的pH,室温下,使溶液中杂质离子刚好沉淀完全而全部除去(浓度小于1.0×10-5mol•L-1).需调节溶液pH范围为5.0<pH<7.3.
(3)充分焙烧的化学方程式为4CoC2O4?2H2O+3O2$\frac{\underline{\;焙烧\;}}{\;}$2Co2O3+8 H2O+8CO2.
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见下表.操作2中,蒸发浓缩后必须趁热过滤,其原因是减少Li2CO3的溶解损失.
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
(6)①用Li、Co形成某锂离子电池的正极是LiCoO2,含Li+导电固体为电解质.充电时,Li+还原为Li,并以原子形式嵌入电池负极材料碳-6(C6)中(如图a).电池反应为LixC6+Li1-xCoO2$?_{充电}^{放电}$C6+LiCoO2,
写出该电池放电时的负极反应式LixC6-xe-=C6+xLi+.
②锂硫电池的总反应为:2Li+S$?_{充电}^{放电}$Li2S,图b表示用锂离子电池给锂硫电池充电,请在图b的电极
 中填写“Li”或“S”,以达到给锂硫电池充电的目的.
中填写“Li”或“S”,以达到给锂硫电池充电的目的.
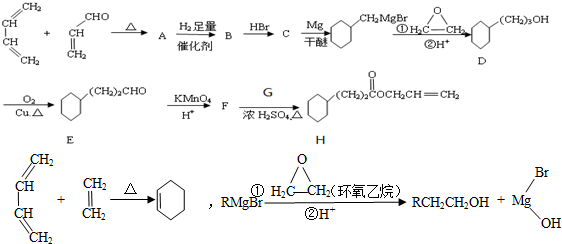
 ,G物质核磁共振氢谱共有4个峰.
,G物质核磁共振氢谱共有4个峰. .写出D生成E的化学方程式
.写出D生成E的化学方程式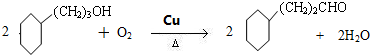 .
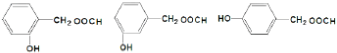
.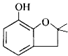 呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式:
呋喃酚是一种合成农药的重要中间体,它的同分异构体很多,写出符合下列条件的所有芳香族同分异构体的结构简式: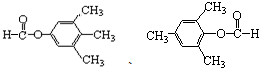 .
.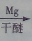 CH3CH2MgBr
CH3CH2MgBr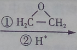 CH3CH2CH2CH2OH.
CH3CH2CH2CH2OH.

 扁桃酸是重要的医药和染料中间体,其应用非常广泛.扁桃酸的结构简式如图所示.
扁桃酸是重要的医药和染料中间体,其应用非常广泛.扁桃酸的结构简式如图所示.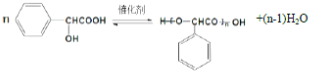 .
. .
.