2.化学反应速率与化学反应限度相关知识在化工生产中应用广泛.
Ⅰ.一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:
N2(g)+3H2O(g)?2NH3(g)+$\frac{3}{2}$O2(g)△H>0,进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
请回答下列问题:
(1)50℃时从开始到3h内以O2物质的量变化表示的平均反应速率为1.5×10-6mol•h-1.
(2)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢.下列措施既可增加反应速率又可以增加NH3产率的是A(填序号).
A.升高温度 B.将NH3从体系中分离
C.恒容条件下,充入He D.加入合适的催化剂
(3)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.在某10L恒容的密闭容器中加入2molN2和4molH2,达到平衡时放出的热量为92.4KJ,该条件下的平衡常数为400.下列能判断该反应一定达到平衡状态的是AD(填序号).
A.容器中气体的平均相对分子质量不随时间而变化
B.2v正(NH3)═3v逆(H2)
C.N2、H2、NH3三种物质的反应速率之比为1:3:2
D.容器中总压强不随时间而变化
E.反应的△H不再变化
Ⅱ.高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的△H<0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡.求CO的平衡转化率=60%;欲提高(2)中CO的平衡转化率,可采取的措施是C(填序号).
(3)下列措施中能使平衡时$\frac{c(CO)}{c({CO}_{2})}$增大的是D(填序号).
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.提高反应温度 E.减小容器的体积 F.加入合适的催化剂.
Ⅰ.一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:
N2(g)+3H2O(g)?2NH3(g)+$\frac{3}{2}$O2(g)△H>0,进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
| T/℃ | 30 | 40 | 50 |
| 生成 NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
(1)50℃时从开始到3h内以O2物质的量变化表示的平均反应速率为1.5×10-6mol•h-1.
(2)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢.下列措施既可增加反应速率又可以增加NH3产率的是A(填序号).
A.升高温度 B.将NH3从体系中分离
C.恒容条件下,充入He D.加入合适的催化剂
(3)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ/mol.在某10L恒容的密闭容器中加入2molN2和4molH2,达到平衡时放出的热量为92.4KJ,该条件下的平衡常数为400.下列能判断该反应一定达到平衡状态的是AD(填序号).
A.容器中气体的平均相对分子质量不随时间而变化
B.2v正(NH3)═3v逆(H2)
C.N2、H2、NH3三种物质的反应速率之比为1:3:2
D.容器中总压强不随时间而变化
E.反应的△H不再变化
Ⅱ.高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的△H<0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡.求CO的平衡转化率=60%;欲提高(2)中CO的平衡转化率,可采取的措施是C(填序号).
(3)下列措施中能使平衡时$\frac{c(CO)}{c({CO}_{2})}$增大的是D(填序号).
A.减少Fe的量 B.增加Fe2O3的量 C.移出部分CO2 D.提高反应温度 E.减小容器的体积 F.加入合适的催化剂.
18.将TiO2转化为TiCl4是工业冶炼金属钛的主要反应之一.已知:
TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140.5kJ?mol-1
C(s,石墨)+O2(g)═CO2(g)△H=-110.5kJ?mol-1
则反应TiO2(s)+2Cl2(g)+C(s,石墨)═TiCl4(l)+CO2(g)的△H是( )
TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140.5kJ?mol-1
C(s,石墨)+O2(g)═CO2(g)△H=-110.5kJ?mol-1
则反应TiO2(s)+2Cl2(g)+C(s,石墨)═TiCl4(l)+CO2(g)的△H是( )
| A. | +30.0kJ?mol-1 | B. | -80.5kJ?mol-1 | C. | -30.0kJ?mol-1 | D. | +80.5kJ?mol-1 |
17.在同温同压下,下列各组热化学方程式中Q2>Q1的是( )
0 152195 152203 152209 152213 152219 152221 152225 152231 152233 152239 152245 152249 152251 152255 152261 152263 152269 152273 152275 152279 152281 152285 152287 152289 152290 152291 152293 152294 152295 152297 152299 152303 152305 152309 152311 152315 152321 152323 152329 152333 152335 152339 152345 152351 152353 152359 152363 152365 152371 152375 152381 152389 203614
| A. | 2H2(g)+O2(g)═2H2O(g)△H=-Q1 2H2(g)+O2(g)═2H2O(l)△H=-Q2 | |
| B. | S(g)+O2(g)═SO2(g)△H=-Q1 S(s)+O2(g)═SO2(g)△H=-Q2 | |
| C. | C(s)+O2(g)═CO2(g)△H=-Q1 C(s)+$\frac{1}{2}$O2(g)═CO(g)△H=-Q2 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H=-Q1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-Q2 |
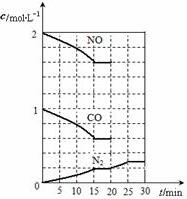 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.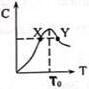 将物质的量均为3.00mol物质A、B混合于L容器中,发生如下反应3A+B?2C,再反应过程中C的物质的量分数随温度变化如图所示:
将物质的量均为3.00mol物质A、B混合于L容器中,发生如下反应3A+B?2C,再反应过程中C的物质的量分数随温度变化如图所示: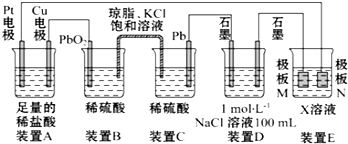
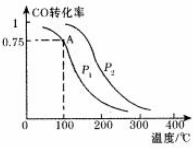 CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法.
CO、SO2是主要的大气污染气体,利用化学反应原理是治理污染的重要方法.