题目内容
14.在一密闭的2L的容器里充入8molSO2和4mol18O2,在一定条件下开始反应:2SO2(g)+O2(g)?2SO3(g),在2min末测得容器中有7.2molSO2.试回答:①反应后18O原子存在哪些物质中SO2、O2、SO3;
②2min末SO3的浓度0.4mol/L;
③用O2的浓度变化表示该时间段内的化学反应速率:v(O2)=0.1mol/(L.min).
分析 ①反应本质是旧键断裂形成原子,原子再相互组合形成新物质,该反应属于可逆反应;
②计算参加反应二氧化硫物质的量,再结合方程式计算三氧化硫物质的量,根据c=$\frac{n}{V}$计算;
③根据v=$\frac{△c}{△t}$计算v(SO2),再利用速率之比等于其化学计量数之比计算v(O2).
解答 解:①反应本质是旧键断裂形成原子,原子再相互组合形成新物质,该反应属于可逆反应,故反应后SO2、O2、SO3中均含有18O原子,
故答案为:SO2、O2、SO3;
②2min内参加反应二氧化硫物质的量为8mol-7.2mol=0.8mol,由方程式可知生成三氧化硫为0.8mol,故2min末SO3的浓度为$\frac{0.8mol}{2L}$=0.4mol/L,
故答案为:0.4mol/L;
③2min内v(SO2)=$\frac{\frac{0.8mol}{2L}}{2min}$=0.2mol/(L.min),速率之比等于其化学计量数之比,则v(O2)=$\frac{1}{2}$v(SO2)=0.1mol/(L.min),
故答案为:0.1mol/(L.min).
点评 本题考查可逆反应特征、化学平衡计算、反应速率计算,比较基础,通常利用定义式与速率规律计算反应速率.

练习册系列答案
相关题目
2.月球的矿产资源极为丰富,仅月面表层5cm厚的沙土中就含铁单质上亿吨,月球上的主要矿物有辉石[CaMgSi2O6]、斜长石[KAlSi3O8]和橄榄石[(Mg或Fe)2SiO4]等,下列说法或分析不正确的是( )
| A. | 辉石、斜长石及橄榄石均属于硅酸盐矿 | |
| B. | 橄榄石中铁为+2价 | |
| C. | 月球表层沙土中有游离态铁是因为月球的表面几乎没有氧气 | |
| D. | 斜长石的氧化物形式可表示为:K2O•Al2O3•3SiO2 |
9.下列叙述符合平衡移动原理的是( )
| A. | 向FeCl3+3KSCN?Fe(SCN)3+3KCl平衡体系中,加入KCl固体,溶液颜色加深 | |
| B. | 对2NO2?N2O4的平衡体系增大压强,平衡后气体颜色变浅 | |
| C. | 对H2(g)+I2(g)?2HI(g)的平衡体系增大压强,容器内气体颜色变深 | |
| D. | 向滴有石蕊的醋酸溶液中通入HCl气体,溶液颜色加深 |
6.爱迪生电池在充电和放电时发生的反应:Fe+NiO2+2H2O?Fe(OH)2+Ni(OH)2,下列该蓄电池推断不正确的是( )
| A. | 放电时,Fe参与负极反应,NiO2参与正极反应 | |
| B. | 充电时,阴极上的电极反应式为:Fe(OH)2+2e-═Fe+2OH- | |
| C. | 蓄电池的电极必须浸入某种碱性电解质溶液中 | |
| D. | 放电时,电解质溶液中的阴离子向正极方向移动 |
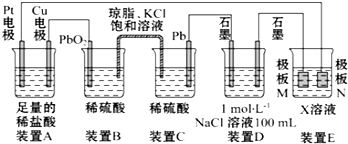
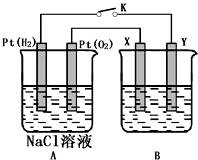 某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题:
某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题: