下列有关元素的性质及其递变规律,说法正确的是( )
| A、短周期元素都是主族元素 |
| B、第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| C、构成单质的分子中一定含有共价键 |
| D、硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
下列叙述不正确的是( )
| A、金属腐蚀的本质是金属原子失去电子而被氧化 |
| B、将地下钢管与直流电源的正极相连,用来保护钢管 |
| C、电解饱和食盐水制氢氧化钠,可以用铁做阴极 |
| D、氢氧燃料电池中,氢气在负极发生氧化反应 |
下列金属需密封保存的是( )
| A、Na | B、Mg | C、Al | D、Cu |
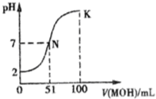 常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、HA为一元强酸 | ||
| B、N点水的电离程度小于K点水的电离程度 | ||
C、随着MOH溶液的滴加,比值
| ||
| D、若K点对应的溶液的PH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L |
将pH=3的硫酸溶液和pH=10的氢氧化钠溶液相混合,若要使混合后溶液的pH=7,则硫酸溶液和氢氧化溶液的体积比约为( )
| A、1:2 | B、1:9 |
| C、1:10 | D、1:20 |
下列说法正确的是( )
| A、淀粉、纤维素、油脂都属于高分子化合物 |
| B、油脂水解得到的醇是丙三醇 |
| C、酶只有在强酸性或强碱性条件下才能发挥作用 |
| D、可溶性铜盐可以使蛋白质产生盐析 |
下列化学反应的有机产物中,存在同分异构体的是( )
| A、(CH3)2CHCH2Br在碱性溶液中水解 |
| B、苯在催化剂FeCl3作用下与Cl2反应 |
C、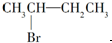 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 |
D、 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
下列有关热化学方程式的叙述中,正确的是( )
| A、含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(1)△H=+57.3kJ/mol | ||
| B、已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | ||
| C、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,则氢气的燃烧热为241.8kJ | ||
D、已知C(s)+O2(g)=CO2(g)△H1;C(s)+
|
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、80g硝酸铵含有氮原子数为2NA |
| B、1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA |
| C、标准状况下,11.2L SO3所含分子数为0.5 NA |
| D、0.1mol FeCl3加入沸水中,全部制得Fe(OH)3胶体,胶体粒子数为0.1NA |
10mL 0.05mol/L含有R2O72-离子的浓溶液恰好能将60mL 0.05mol/L的Fe2+溶液完全氧化,则元素R在还原产物中的化合价为( )
| A、+1价 | B、+2价 |
| C、+3价 | D、+6价 |